Как самостоятельно поднять плотность электролита в автомобильном аккумуляторе — что делать если упала плотность в АКБ
Любой автомобильный аккумулятор является кислотным элементом. В нем содержится раствор серной кислоты определенной плотности. Он выполняет роль катализатора процесса преобразования чистого свинца, его оксида и кислоты в воду и сульфат свинца в процессе разряда и зарядки. Если концентрация кислоты окажется меньше, батарея будет выдавать меньше мощности. В этой статье мы рассмотрим, как поднять плотность электролита и на что она влияет.
Особенности химического процесса в аккумуляторе
В аккумуляторе свинцово-кислотного типа химический процесс стоит в основе его работы. Его интенсивность, в свою очередь, напрямую зависит от конструкции АКБ. В ранних моделях использовался чистый свинец для изготовления электродных решеток и токовых выводов, но это делало их очень мягкими и недолговечными. Для повышения надежности решеток производители стали добавлять в сплав сурьму. Ее массовая доля составляет не более 6%, что очень важно. Введение данного металла несколько снизило эффективность работы аккумулятора, но сделало решетки долговечнее.
Ее массовая доля составляет не более 6%, что очень важно. Введение данного металла несколько снизило эффективность работы аккумулятора, но сделало решетки долговечнее.
Окисляется свинцово-сурьмянистый сплав исключительно из-за состава электролита. С одной стороны, он играет роль катализатора, обеспечивающего работоспособность реакции. А с другой, при несоблюдении концентрации она приносит вред источнику питания в целом. И на многое влияет именно плотность электролита в аккумуляторе, которая в зависимости от состояния заряда постоянно меняется.
Итак, что мы имеем. Свинцовые отрицательные пластины из сплава на 6% из сурьмы, которые погружены в раствор из воды и серной кислоты, также есть положительные пластины с пастой из оксида свинца. В одном 12-вольтовом аккумуляторе 6 банок, в каждой из которых находится комплект отрицательных и положительных пластин. Банки разделены между собой для исключения короткого замыкания между ячейками. Контактная пара взаимодействует между собой через электролит, который обеспечивает перемещение от одного электрода к другому заряженных частиц при подключении нагрузки.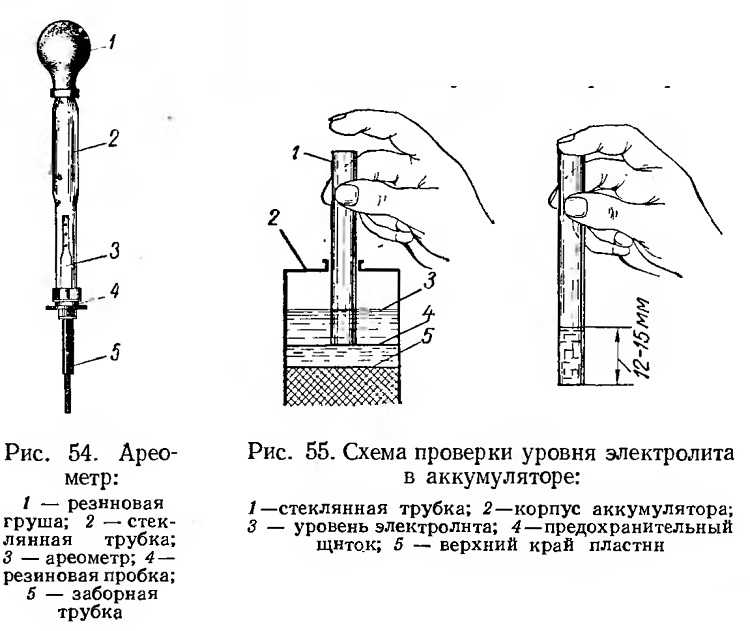 Соответственно, при разряде выделяются вода и сульфат свинца, а при заряде происходит восстановление электродов до своего исходного состояния.
Соответственно, при разряде выделяются вода и сульфат свинца, а при заряде происходит восстановление электродов до своего исходного состояния.
Почему меняется плотность?
Плотность электролита АКБ напрямую зависит от состояния заряда, и она измеряется в количестве чистой серной кислоты в 1 см3 дистиллированной воды. Постепенно, по мере разрядов и неполной зарядки происходит двойное преобразование химического вещества из одной формы в другую. И обратно реакция протекает не так чисто, как в прямом. Частично сульфат свинца остается и постепенно накапливается на решетках, что приводит к сульфатации пластин. Соответственно, количество чистой восстановленной серной кислоты в аккумуляторе становится меньше на единицу объема воды. Изменяющаяся плотность электролита — это обычный химический процесс, который протекает регулярно во время работы источника питания, но в нем могут возникать определенные нарушения.
Снизить интенсивность изменения плотности электролита в аккумуляторе можно только снижением интенсивности разряда батареи. Но в автомобиле это предусмотреть тяжело, поэтому остается только правильно эксплуатировать источник питания и в нужный момент производить его нормальную дозарядку. Стоит отметить, что в нормальной АКБ в процессе разряда и заряда плотность изменяется несущественно, но в измеряемых диапазонах. Например, если оставить фары включенными на ночь, то нормальная плотность 1,4 г/см3 снизится до 1,12 г/см3. А это значение практически равно плотности обычной воды, так как в нормальном растворе количество серной кислоты не превышает 35% от общего объема электролита.
Но в автомобиле это предусмотреть тяжело, поэтому остается только правильно эксплуатировать источник питания и в нужный момент производить его нормальную дозарядку. Стоит отметить, что в нормальной АКБ в процессе разряда и заряда плотность изменяется несущественно, но в измеряемых диапазонах. Например, если оставить фары включенными на ночь, то нормальная плотность 1,4 г/см3 снизится до 1,12 г/см3. А это значение практически равно плотности обычной воды, так как в нормальном растворе количество серной кислоты не превышает 35% от общего объема электролита.
Срок службы
Первые несколько лет в аккумуляторе не наблюдается резкого падения плотности, он заряжается каждый раз после разрядки практически полностью. По разным причинам он начинает недозаряжаться или длительное время стоит без зарядки. Вот тут речь идет уже не просто о падении плотности. Произошла реакция выделения осадка, который уже не способен вступить в химическую реакцию восстановления электрода. Постепенно раствор засоряется этим осадком. Как правило, такое состояние, если в автомобиле с электрикой все в порядке, наступает только после 4-5 лет службы. Если же недозаряд происходит регулярно, то увеличить плотность придется раньше. И делать это можно только с обслуживаемым аккумулятором.
Постепенно раствор засоряется этим осадком. Как правило, такое состояние, если в автомобиле с электрикой все в порядке, наступает только после 4-5 лет службы. Если же недозаряд происходит регулярно, то увеличить плотность придется раньше. И делать это можно только с обслуживаемым аккумулятором.
Как измерить плотность АКБ?
Чтобы узнать, насколько следует повысить плотность АКБ, необходимо ее измерить. В домашних условиях сделать это самостоятельно без специального прибора невозможно. Для проделывания всей этой процедуры потребуется:
- ареометр;
- мерный стакан;
- груша для забора раствора из батареи;
- емкость для приготовления нового раствора;
- кислота или специальный корректирующий электролит.
Наберите раствора в грушу, к которой присоединена стеклянная трубка, а внутри находится прибор. Располагать его нужно так, чтобы ареометр не касался стенок трубки. Со шкалы списывается значение. Если плотность оказывается ниже 1,4/см3, то ее нужно повысить.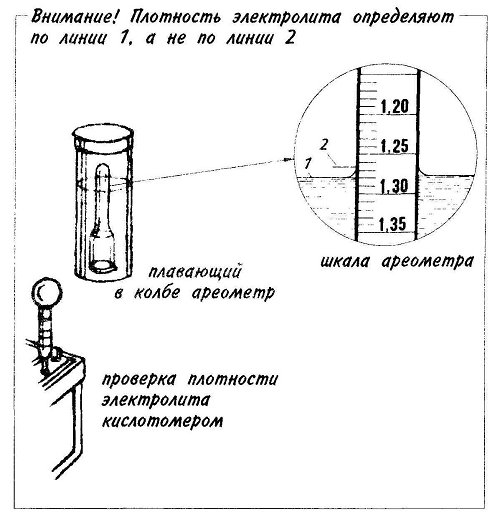 Сделать это можно добавлением корректирующего электролита. Повторное измерение плотности выполняется после получасовой зарядки и 2-часового простоя в покое.
Сделать это можно добавлением корректирующего электролита. Повторное измерение плотности выполняется после получасовой зарядки и 2-часового простоя в покое.
Как восстановить плотность?
Поднять плотность АКБ можно тремя способами:
- залить новый электролит;
- добавить серную кислоту;
- воспользоваться корректирующим электролитом.
Важно учесть, что серная кислота не испаряется. На это при низких температурах до 140 градусов способна только вода, поэтому при низком уровне следует все же доливать воду, а при недостаточной плотности по прибору — кислоту в чистом виде. Ее количество определяется как доля в %. Например, плотность АКБ составляет 1,12 г/см3. Не хватает буквально 0,28 г/см3. Получается, что в недостающем количестве дистиллированной воды нужно разбавить 25-28% от всего нужного объема кислоты и залить в батарею.
Как устроен автомобильный аккумулятор >
Восстановление аккумулятора содой — зачем в АКБ добавляют пищевую соду
16 Feb, 2021
Восстановление аккумулятора содой — способ оживить уставшую батарею, который стал популярен в сети.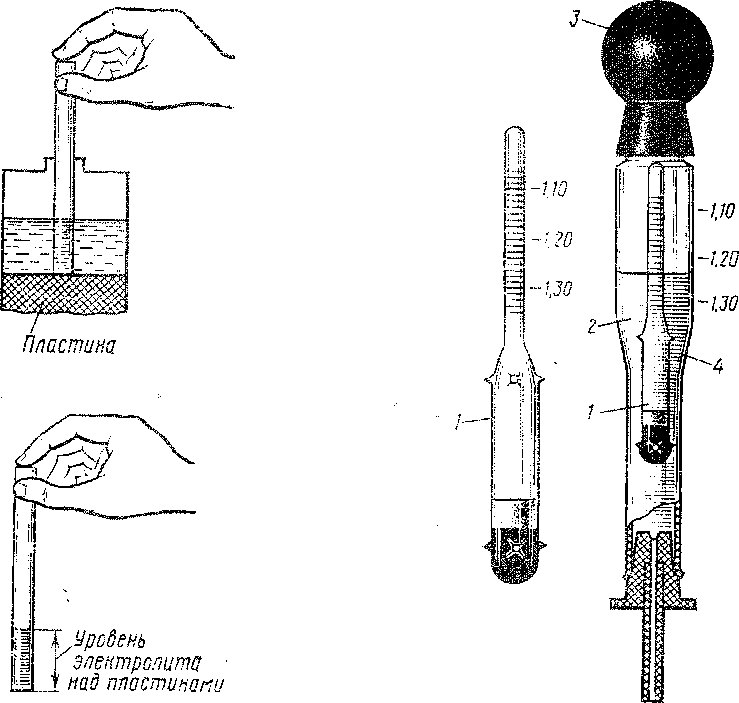 Практически все автолюбители хотя бы раз в жизни сталкивались с тем, что АКБ перестал держать заряд или разрядился полностью и не реагирует на зарядные устройства. В этом случае предлагалось его заменить на новый. Восстановление аккумулятора содой — шанс подарить ему жизнь и сэкономить на покупке замены.
Практически все автолюбители хотя бы раз в жизни сталкивались с тем, что АКБ перестал держать заряд или разрядился полностью и не реагирует на зарядные устройства. В этом случае предлагалось его заменить на новый. Восстановление аккумулятора содой — шанс подарить ему жизнь и сэкономить на покупке замены.
Данный метод возможен только при сульфатации пластин.
Что такое засульфатированная АКБ
Процесс сульфатации — это скопление солей сульфатов на поверхности. Внутри аккумулятора имеются свинцовые пластины и электролит. В процессе химической реакции образуется электричество, которое поступает в стартёр, что приводит в движение автомобиль. В норме плотность электролита — 1.27. Если машина долго не используется, данный показатель снижается. В результате на пластинах образуется скопление солей и батарея выходит из строя.
Данный метод основан на очищении поверхности от них и замены электролита. Отсюда следует, что он эффективен только при этом виде неисправности.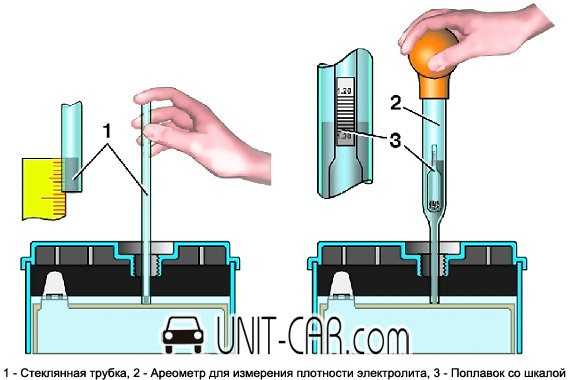
Как восстановить аккумулятор содой
Процедура происходит в несколько этапов:
- Подготовка;
- Промывка;
- Сборка и установка АКБ.
На батарее скручиваются крышки. Старый электролит сливается с помощью шприца в отдельную ёмкость.
Необходимо подготовить раствор соды с дистиллированной водой в пропорции 100 г сухого вещества на 1 литр жидкости. Полученный реагент заливается внутрь АКБ. Реакция происходит моментально. В таком состоянии батарею оставляют на 20 мин. После чего жидкость сливается. Наличие осадка говорит о том, что пластины очистились.
Следующим шагом станет промывка аккумулятора дистиллированной водой и помещение внутрь него старого электролита. После этого жидкость опять сливают. Этот процесс в среднем занимает около 20 минут.
Финальным этапом станет залитие свежего электролита, вместе с которым АКБ нужно поставить на зарядку. Уже через 10 часов можно увидеть показатели в 14 Вольт, с нагрузкой 10. 5.
5.
Эффективность метода
Популярность способа восстановления аккумулятора пищевой содой своими руками растет. Но так ли все просто и действенно?
Для его оценки нужно понимать суть процесса химических реакций и устройство самого АКБ. Пластины внутри батареи не зафиксированы. При переворачивании аккумулятора они меняют положение, что приводит к механическим повреждениям. Свинцово-кислотные батареи должны всегда находиться в одном положении. Их смещение приводит к необратимым последствиям. Уже на этом этапе к данной методике у специалистов появляется много вопросов.
Ещё одним спорным моментом считается само использование пищевой соды для промывки аккумулятора. Дело в том, что свинцовые пластины покрыты специальным веществом, вступающим в реакцию с электролитом. Оно имеет пористую структуру. При попадании на него содового раствора, соду нельзя до конца вывести. В результате после прочистки и залития нового электролита, она продолжает вступать с ним реакцию. В итоге происходят необратимые процессы, разрушающие аккумулятор.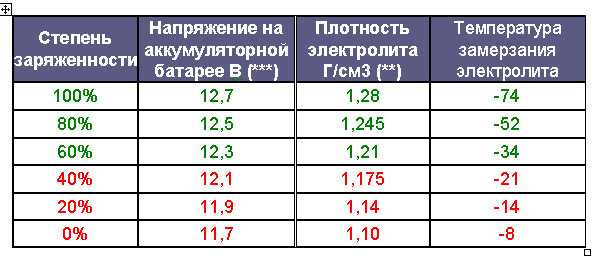
Ещё одним аргументом против является само устройство свинцово-кислотной АКБ. Она имеет неразборный корпус. Увидеть состояние деталей внутри не представляется возможным. В итоге сам факт сульфатации остаётся предположением. Причина поломки может быть иная.
Уставший аккумулятор нужно периодически заряжать. Волшебных средств, дарующих ему вторую жизнь не существует. Все работы по восстановлению техники должны проводиться в оборудованных сервисных центрах.
Prev
Next
Восстановление лития и кобальта из отработанных ионно-литиевых аккумуляторов мобильных телефонов
. 2013 сен; 33 (9): 1890-7.
Манис Кумар Джа 1 , Анджан Кумари, Амрита Кумари Джха, Винай Кумар, Джумки Хаит, Банши Дхар Панди
принадлежность
- 1 Отдел извлечения и формовки металлов, CSIR – Национальная металлургическая лаборатория, Джамшедпур 831 007, Индия.
 [email protected]
[email protected]
- PMID: 23773705
- DOI: 10.1016/j.wasman.2013.05.008
. 2013 сен; 33 (9): 1890-7.
doi: 10.1016/j.wasman.2013.05.008. Epub 2013 14 июня.
Авторы
Манис Кумар Джа 1 , Анджан Кумари, Амрита Кумари Джха, Винай Кумар, Джумки Хаит, Банши Дхар Панди
принадлежность
- 1 Отдел извлечения и формовки металлов, CSIR – Национальная металлургическая лаборатория, Джамшедпур 831 007, Индия.
 [email protected]
[email protected]
- PMID: 23773705
- DOI: 10.1016/j.wasman.2013.05.008
Абстрактный
Ввиду строгих экологических норм, наличия ограниченных природных ресурсов и постоянно растущей потребности в критических элементах альтернативной энергии сообщается об экологически безопасном процессе выщелачивания для извлечения лития и кобальта из катодных активных материалов отработанных литий-ионных аккумуляторов. мобильных телефонов. Были проведены эксперименты по оптимизации технологических параметров извлечения лития и кобальта путем варьирования концентрации выщелачивателя, плотности пульпы, объема восстановителя и температуры. Выщелачивание 2М серной кислотой с добавкой 5% H(2)O(2) (об.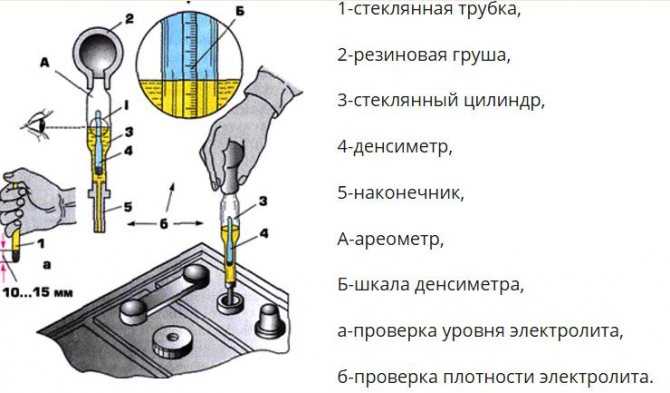
Ключевые слова: кобальт; выщелачивание; литий; Переработка.
Copyright © 2013 Elsevier Ltd. Все права защищены.
Похожие статьи
Извлечение кобальта и лития из отработанных литий-ионных аккумуляторов с использованием органической лимонной кислоты в качестве выщелачивателя.

Ли Л, Гэ Дж, Ву Ф, Чен Р, Чен С, Ву Б. Ли Л и др. Джей Хазард Матер. 2010 15 апреля; 176 (1-3): 288-93. doi: 10.1016/j.jhazmat.2009.11.026. Epub 2009 11 ноября. Джей Хазард Матер. 2010. PMID: 19954882
Устойчивый процесс восстановления ценных металлов из отработанных литий-ионных аккумуляторов.
Фан Б., Чен С., Чжоу Т., Чжан Дж., Сюй Б. Фан Б и др. Управление отходами Res. 2016 май; 34(5):474-81. дои: 10.1177/0734242X16634454. Epub 2016 7 марта. Управление отходами Res. 2016. PMID: 26951340
Органический оксалат как выщелачиватель и осадитель для извлечения ценных металлов из отработанных литий-ионных аккумуляторов.
Сунь Л., Цю К. Сан Л. и др. Управление отходами.
 2012 авг; 32 (8): 1575-82. doi: 10.1016/j.wasman.2012.03.027. Epub 2012 23 апр.
Управление отходами. 2012.
PMID: 22534072
2012 авг; 32 (8): 1575-82. doi: 10.1016/j.wasman.2012.03.027. Epub 2012 23 апр.
Управление отходами. 2012.
PMID: 22534072Биовыщелачивание лития: новый подход к извлечению лития из отработанных литий-ионных аккумуляторов.
Моаззам П., Боруманд Ю., Рабии П., Багбадерани С.С., Мокарян П., Мохагегян Ф., Мохаммед Л.Дж., Размжу А. Моаззам П. и др. Хемосфера. 2021 авг; 277:130196. doi: 10.1016/j.chemosphere.2021.130196. Epub 2021 6 марта. Хемосфера. 2021. PMID: 33784558 Обзор.
Методы восстановления и статус регулирования отработанных литий-ионных аккумуляторов в Китае: мини-обзор.
Siqi Z, Guangming L, Wenzhi H, Juwen H, Haochen Z. Сики З. и др. Управление отходами Res. 2019Ноябрь; 37 (11): 1142-1152.
 дои: 10.1177/0734242X19857130. Epub 2019 27 июня.
Управление отходами Res. 2019.
PMID: 31244410
Обзор.
дои: 10.1177/0734242X19857130. Epub 2019 27 июня.
Управление отходами Res. 2019.
PMID: 31244410
Обзор.
Посмотреть все похожие статьи
Цитируется
Синтез и фазовое поведение платформы CO 2 — Растворимые функциональные градиентные сополимеры, содержащие металлокомплексообразующие звенья.
Руйу А., Буйак С., Химелло О., Содо-Пирулей К., Сенила М., Яниш Т., Лакруа-Демазес П. Руиу А. и др. Полимеры (Базель). 2022 30 июня;14(13):2698. doi: 10.3390/polym14132698. Полимеры (Базель). 2022. PMID: 35808744 Бесплатная статья ЧВК.
Оценка методов и процессов переработки литий-ионных аккумуляторов.
Макваримба С.П., Тан М., Пэн Ю., Лу С.
 , Чжэн Л., Чжао З., Чжэнь А.Г.
Макваримба С.П. и соавт.
iНаука. 2022 28 апреля; 25 (5): 104321. doi: 10.1016/j.isci.2022.104321. Электронная коллекция 2022 20 мая.
iНаука. 2022.
PMID: 35602951
Бесплатная статья ЧВК.
Обзор.
, Чжэн Л., Чжао З., Чжэнь А.Г.
Макваримба С.П. и соавт.
iНаука. 2022 28 апреля; 25 (5): 104321. doi: 10.1016/j.isci.2022.104321. Электронная коллекция 2022 20 мая.
iНаука. 2022.
PMID: 35602951
Бесплатная статья ЧВК.
Обзор.Сбор лития из наиболее распространенных первичных и вторичных источников: сравнительное исследование традиционных и мембранных технологий.
Батт Ф.С., Льюис А., Чен Т., Мазлан Н.А., Вэй Х., Хайер Дж., Чен С., Хан Дж., Ян И., Ян С., Хуан Ю. Батт Ф.С. и др. Мембраны (Базель). 2022 29 марта; 12 (4): 373. doi: 10.3390/membranes12040373. Мембраны (Базель). 2022. PMID: 35448344 Бесплатная статья ЧВК. Обзор.
Новый способ переработки отработанных литий-ионных аккумуляторов.
Пинна Э.
 Г., Торо Н., Гальегос С., Родригес М.Х.
Пинна Э.Г. и соавт.
Материалы (Базель). 2021 22 декабря; 15 (1): 44. дои: 10.3390/ma15010044.
Материалы (Базель). 2021.
PMID: 35009191
Бесплатная статья ЧВК.
Г., Торо Н., Гальегос С., Родригес М.Х.
Пинна Э.Г. и соавт.
Материалы (Базель). 2021 22 декабря; 15 (1): 44. дои: 10.3390/ma15010044.
Материалы (Базель). 2021.
PMID: 35009191
Бесплатная статья ЧВК.Текущий процесс переработки отработанных литий-ионных аккумуляторов.
Чжоу Л.Ф., Ян Д., Ду Т., Гонг Х., Луо В.Б. Чжоу Л.Ф. и др. Фронт хим. 2020 3 декабря; 8: 578044. doi: 10.3389/fchem.2020.578044. Электронная коллекция 2020. Фронт хим. 2020. PMID: 33344413 Бесплатная статья ЧВК. Обзор.
Типы публикаций
термины MeSH
вещества
Университет мощных литий-ионных аккумуляторов
ПРИМЕЧАНИЕ : Эта статья была заархивирована .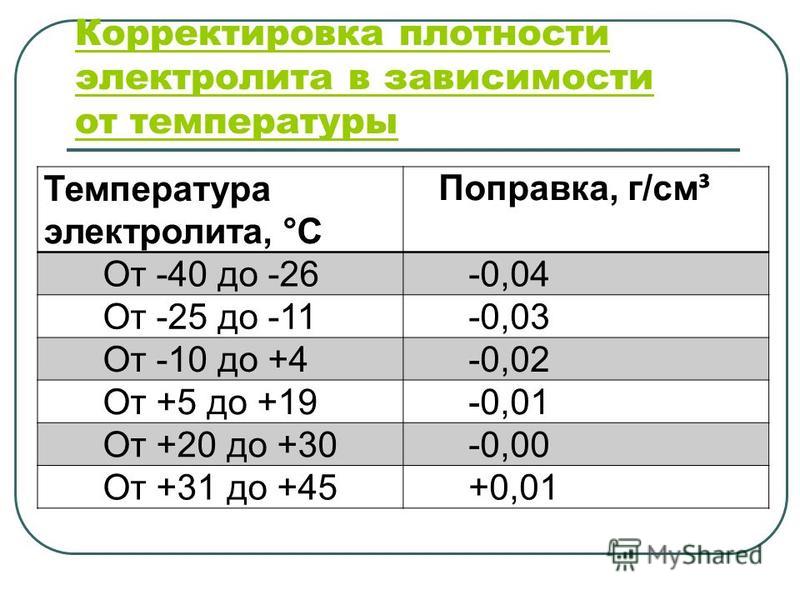 Пожалуйста, ознакомьтесь с нашей новой версией «Типы литий-ионных аккумуляторов».
Пожалуйста, ознакомьтесь с нашей новой версией «Типы литий-ионных аккумуляторов».
Большинство литий-ионных аккумуляторов для портативных устройств изготовлены на основе кобальта. Система состоит из положительного электрода из оксида кобальта (катода) и графитового углерода в отрицательном электроде (аноде). Одним из основных преимуществ батареи на основе кобальта является ее высокая плотность энергии. Длительное время работы делает эту химию привлекательной для мобильных телефонов, ноутбуков и фотоаппаратов.
Широко используемый литий-ионный на основе кобальта имеет недостатки; он предлагает относительно низкий ток разряда. Большая нагрузка приведет к перегреву рюкзака, что поставит под угрозу его безопасность. Цепь безопасности батареи на основе кобальта обычно ограничивается скоростью заряда и разряда около 1С. Это означает, что элемент 18650 емкостью 2400 мАч можно заряжать и разряжать только максимальным током 2,4 А. Другим недостатком является увеличение внутреннего сопротивления, которое происходит при езде на велосипеде и старении. Через 2-3 года использования аккумулятор часто приходит в негодность из-за большого падения напряжения под нагрузкой, вызванного большим внутренним сопротивлением. Рисунок 1 иллюстрирует кристаллическую структуру оксида кобальта. Другим недостатком является увеличение внутреннего сопротивления, которое происходит при езде на велосипеде и старении. Через 2-3 года использования аккумулятор часто приходит в негодность из-за большого падения напряжения под нагрузкой, вызванного большим внутренним сопротивлением. Рисунок 1 иллюстрирует кристаллическую структуру оксида кобальта. | |
| Рис. 1. Катод из кристаллического оксида лития-кобальта имеет «слоистую» структуру . Ионы лития показаны связанными с оксидом кобальта. Во время разряда ионы лития перемещаются от катода к аноду. Поток меняет направление при зарядке. |
В 1996 году ученым удалось использовать оксид лития-марганца в качестве катодного материала. Это вещество образует трехмерную структуру шпинели, улучшающую ионный поток между электродами. Высокий поток ионов снижает внутреннее сопротивление и увеличивает нагрузочную способность. Сопротивление остается низким при циклировании, однако батарея стареет, а общий срок службы аналогичен сроку службы кобальта. Шпинель по своей природе обладает высокой термической стабильностью и требует меньше схем безопасности, чем кобальтовая система. Низкое внутреннее сопротивление ячейки является ключом к высокой производительности. Эта характеристика дает преимущества при быстрой зарядке и сильноточной разрядке. Литий-ионный аккумулятор на основе шпинели в ячейке 18650 может разряжаться при токе 20-30А с минимальным тепловыделением. Допускаются короткие односекундные импульсы нагрузки, вдвое превышающие указанный ток. Некоторое накопление тепла невозможно предотвратить, и температура ячейки не должна превышать 80°C. Высокий поток ионов снижает внутреннее сопротивление и увеличивает нагрузочную способность. Сопротивление остается низким при циклировании, однако батарея стареет, а общий срок службы аналогичен сроку службы кобальта. Шпинель по своей природе обладает высокой термической стабильностью и требует меньше схем безопасности, чем кобальтовая система. Низкое внутреннее сопротивление ячейки является ключом к высокой производительности. Эта характеристика дает преимущества при быстрой зарядке и сильноточной разрядке. Литий-ионный аккумулятор на основе шпинели в ячейке 18650 может разряжаться при токе 20-30А с минимальным тепловыделением. Допускаются короткие односекундные импульсы нагрузки, вдвое превышающие указанный ток. Некоторое накопление тепла невозможно предотвратить, и температура ячейки не должна превышать 80°C. | |
| Рис. 2: Катодный кристалл оксида лития-марганца имеет «трехмерную каркасную структуру» . Эта структура шпинели, которая обычно состоит из ромбовидных форм, соединенных в решетку, появляется после первоначального формирования.  Эта система обеспечивает высокую проводимость, но более низкую плотность энергии. Эта система обеспечивает высокую проводимость, но более низкую плотность энергии. |
| Шпинелевая батарея имеет и недостатки. Одним из наиболее существенных недостатков является меньшая емкость по сравнению с системой на основе кобальта. Шпинель обеспечивает примерно 1200 мАч в корпусе 18650, что примерно вдвое меньше, чем у кобальтового эквивалента. Несмотря на это, шпинель по-прежнему обеспечивает плотность энергии, которая примерно на 50% выше, чем у эквивалента на основе никеля. | Рисунок 3: Формат ячейки 18650. Размеры этой часто используемой ячейки: 18 мм в диаметре и 65 мм в длину. |
Типы литий-ионных аккумуляторов
Литий-ионные аккумуляторы еще не достигли полной зрелости, и технология постоянно совершенствуется. Анод в современных элементах состоит из смеси графита, а катод — из комбинации лития и других выбранных металлов. Следует отметить, что все материалы в батарее имеют теоретическую плотность энергии. С литий-ионным анодом хорошо оптимизирован, и можно добиться небольших улучшений с точки зрения изменений конструкции. Катод, однако, обещает дальнейшие усовершенствования. Поэтому исследования аккумуляторов сосредоточены на материале катода. Еще одна часть, которая имеет потенциал, — это электролит. Электролит служит реакционной средой между анодом и катодом.
Следует отметить, что все материалы в батарее имеют теоретическую плотность энергии. С литий-ионным анодом хорошо оптимизирован, и можно добиться небольших улучшений с точки зрения изменений конструкции. Катод, однако, обещает дальнейшие усовершенствования. Поэтому исследования аккумуляторов сосредоточены на материале катода. Еще одна часть, которая имеет потенциал, — это электролит. Электролит служит реакционной средой между анодом и катодом.
Аккумуляторная промышленность постепенно увеличивает мощность на 8-10% в год. Ожидается, что эта тенденция сохранится. Это, однако, далеко от закона Мура, который определяет удвоение количества транзисторов на кристалле каждые 18-24 месяца. Перевод этого увеличения на батарею будет означать удвоение емкости каждые два года. Вместо двух лет литий-ион удвоил свою энергоемкость за 10 лет.
Современные литий-ионные аккумуляторы бывают разных «вкусов», и различия в составе в основном связаны с материалом катода. В приведенной ниже таблице 1 представлены наиболее часто используемые сегодня на рынке литий-ионные аккумуляторы.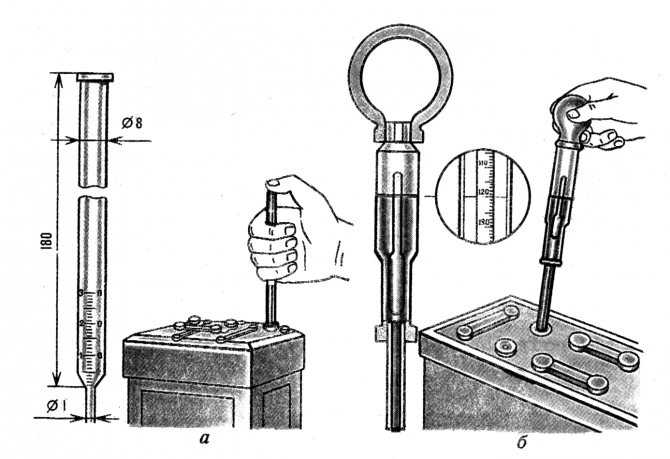 Для простоты мы объединяем химические вещества в четыре группы: кобальт, марганец, NCM и фосфат.
Для простоты мы объединяем химические вещества в четыре группы: кобальт, марганец, NCM и фосфат.
Chemical name | Material | Abbreviation | Short form | Notes | ||
Lithium Cobalt Oxide 1 Также кобальт лития или литий-ион-кобальт) | LiCoO 2 | LCO | Литий-кобальт | Высокая производительность; for cell phone laptop, camera | ||
Lithium | LiMn 2 O 4 | LMO | Литий-марганец или шпинель | Самый безопасный; меньшая емкость, чем у литий-кобальта, но высокая удельная мощность и длительный срок службы. Электроинструменты, | ||
Lithium | LiFePO 4 | LFP | Li-phosphate | |||
Lithium Nickel Manganese Cobalt Oxide 1 , также оксид лития-марганца-кобальта | LiNiMnCoO 2 | NMC | NMC | |||
Lithium Nickel Cobalt Aluminum Oxide 1 | LiNiCoAlO 2 | NCA | NCA | Приобретение значения | LTO | LI-TITANATE |
9 9006
9 9006.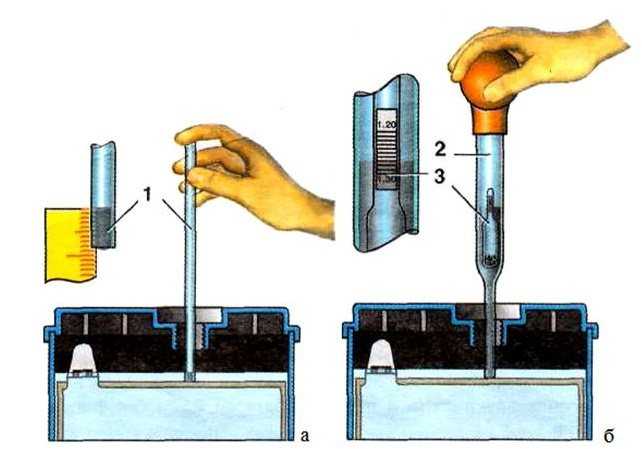 При необходимости мы будем использовать краткую форму.
При необходимости мы будем использовать краткую форму.
1 Материал катода
2 Материал анода
Литий-ионный литий-ионный аккумулятор на основе кобальта впервые появился в 1991 году и был представлен Sony. Эта химия батареи получила быстрое признание из-за ее высокой плотности энергии. Возможно, из-за более низкой плотности энергии литий-ион на основе шпинели имел более медленный старт. При появлении в 1996 мир требовал более длительного времени работы больше всего на свете. Из-за необходимости высокой скорости тока на многих портативных устройствах шпинель теперь вышла на передний план и пользуется большим спросом. Требования настолько велики, что производители, выпускающие эти батареи, не в состоянии удовлетворить спрос. Это одна из причин, почему так мало рекламы делается для продвижения этого продукта. E-One Moli Energy (Канада) — ведущий производитель литий-ионной шпинели цилиндрической формы. Они специализируются на форматах ячеек 18650 и 26700.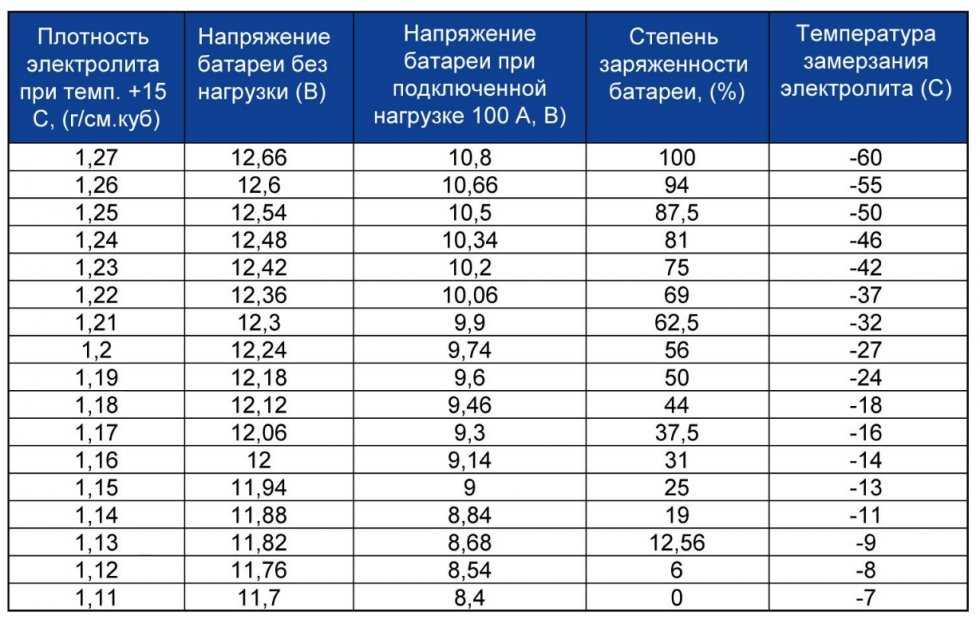 Другими крупными производителями литий-ионных аккумуляторов на основе шпинели являются Sanyo, Panasonic и Sony.
Другими крупными производителями литий-ионных аккумуляторов на основе шпинели являются Sanyo, Panasonic и Sony.
Sony уделяет особое внимание никель-кобальт-марганцевой (NCM) версии. Катод включает в себя кобальт, никель и марганец в кристаллической структуре, которая образует многометаллический оксидный материал, к которому добавлен литий. Производитель предлагает ряд различных продуктов в рамках этого семейства аккумуляторов, предназначенных для пользователей, которым требуется либо высокая плотность энергии, либо высокая нагрузочная способность. Следует отметить, что эти два атрибута нельзя было совмещать в одном и том же пакете; между ними есть компромисс. Обратите внимание, что NCM заряжается до 4,10 В на элемент, что на 100 мВ ниже, чем у кобальта и шпинели. Зарядка этой батареи до 4,20 В на элемент обеспечит более высокую емкость, но срок службы будет сокращен. Вместо обычных 800 циклов, достигаемых в лабораторных условиях, количество циклов сократится примерно до 300.
Новейшим дополнением к семейству литий-ионных аккумуляторов является система A123, в которой в катод добавляются нанофосфатные материалы. Утверждается, что он имеет самую высокую удельную мощность в Вт / кг среди имеющихся в продаже литий-ионных аккумуляторов. Элемент может непрерывно разряжаться до 100% глубины разряда при температуре 35°C и может выдерживать импульсы разряда до 100°C. Система на основе фосфатов имеет номинальное напряжение около 3,3 В на элемент, а пиковое напряжение заряда составляет 3,60 В. Это ниже, чем у литий-ионной батареи на основе кобальта, и для батареи потребуется специальное зарядное устройство. Компания Valance Technology была первой, кто начал коммерциализацию литий-ионных аккумуляторов на основе фосфатов, и их элементы продаются под маркой Saphion.
На Рисунке 4 мы сравниваем плотность энергии (Втч/кг) трех литий-ионных химических элементов и сопоставляем их с традиционными свинцово-кислотными, никель-кадмиевыми и никель-металлогидридными. Можно увидеть постепенное улучшение марганца и фосфата по сравнению со старыми технологиями. Кобальт обеспечивает самую высокую плотность энергии, но менее термически стабилен и не может обеспечивать большие токи нагрузки.
Можно увидеть постепенное улучшение марганца и фосфата по сравнению со старыми технологиями. Кобальт обеспечивает самую высокую плотность энергии, но менее термически стабилен и не может обеспечивать большие токи нагрузки.
| Рис. 4: Плотность энергии обычных аккумуляторов. |
Определение плотности энергии и плотности мощности
Плотность энергии (Втч/кг) — это показатель того, сколько энергии может удерживать батарея. Чем выше плотность энергии, тем дольше будет время работы. Литий-ионные аккумуляторы с кобальтовыми катодами обеспечивают самую высокую плотность энергии. Типичными приложениями являются сотовые телефоны, ноутбуки и цифровые камеры.
Плотность мощности (Вт/кг) указывает, сколько энергии батарея может обеспечить по требованию. Основное внимание уделяется вспышкам мощности, таким как сверление тяжелой стали, а не времени выполнения.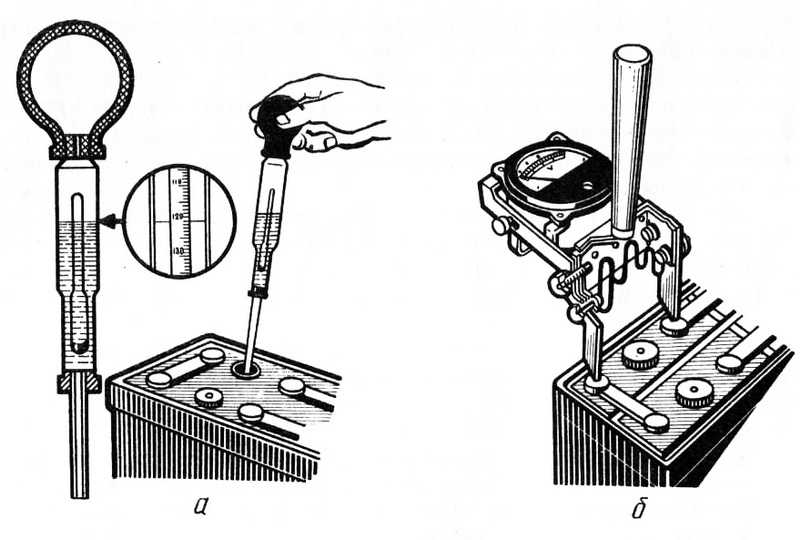 Литий-ионные на основе марганца и фосфата, а также химические вещества на основе никеля являются одними из лучших. Аккумуляторы с высокой удельной мощностью используются для электроинструментов, медицинских приборов и транспортных систем.
Литий-ионные на основе марганца и фосфата, а также химические вещества на основе никеля являются одними из лучших. Аккумуляторы с высокой удельной мощностью используются для электроинструментов, медицинских приборов и транспортных систем.
Можно провести аналогию между плотностью энергии и мощности с бутылкой с водой. Размер бутылки — это плотность энергии, а отверстие — плотность мощности. Большая бутылка может вместить много воды, а большое горлышко может быстро ее наполнить. Большой контейнер с широким горлышком — лучшее сочетание.
Путаница с напряжением
В течение последних 10 лет было известно, что номинальное напряжение литий-ионного аккумулятора составляет 3,60 В на элемент. Это была довольно удобная цифра, потому что она соответствовала трем никелевым батареям (1,2 В на ячейку), соединенным последовательно. Использование более высокого напряжения элемента для литий-ионных аккумуляторов отражает лучшие показания мощности в ватт-часах на бумаге и представляет собой маркетинговое преимущество, однако производитель оборудования будет по-прежнему исходить из того, что элемент рассчитан на 3,60 В.
Номинальное напряжение литий-ионной батареи рассчитывается путем взятия полностью заряженной батареи с напряжением около 4,20 В, полной разрядки ее до напряжения около 3,00 В со скоростью 0,5°C при измерении среднего напряжения.
Из-за более низкого внутреннего сопротивления среднее напряжение системы шпинели будет выше, чем у эквивалента на основе кобальта. Чистая шпинель имеет наименьшее внутреннее сопротивление, а номинальное напряжение ячейки составляет 3,80 В. Исключением снова является литий-ионный на основе фосфата. Эта система больше всего отличается от обычной литий-ионной системы 9.0003
Продление срока службы батареи за счет умеренности
Срок службы батареи дольше при бережном обращении. Высокие зарядные напряжения, чрезмерная скорость заряда и экстремальные условия нагрузки отрицательно сказываются на сроке службы батареи. Долговечность часто является прямым результатом воздействия окружающей среды. Следующие рекомендации предлагают способы продлить срок службы батареи.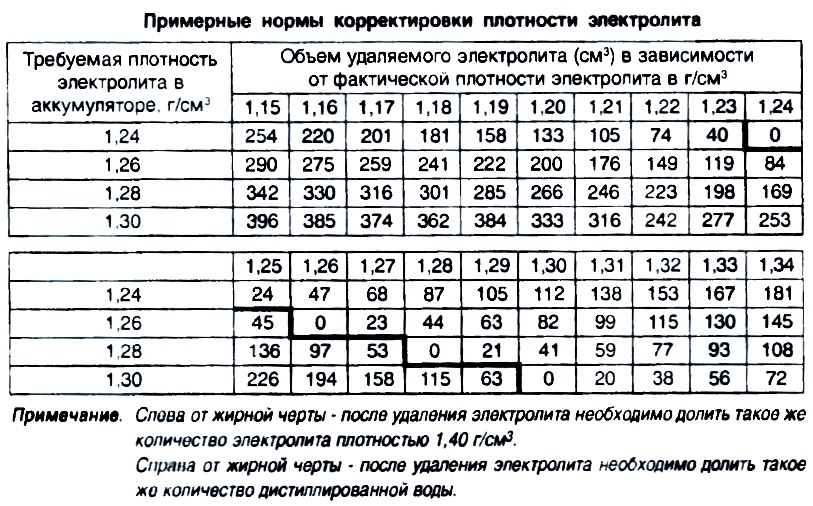
-Время, в течение которого батарея остается на уровне 4,20/ячейка, должно быть как можно короче. Длительное высокое напряжение способствует коррозии, особенно при повышенных температурах. Шпинель менее чувствительна к высокому напряжению.
-3,92 В/ячейка — лучший верхний порог напряжения для литий-ионных аккумуляторов на основе кобальта. Было показано, что зарядка аккумуляторов до этого уровня напряжения удваивает срок службы. Литий-ионные системы для оборонных приложений используют более низкий порог напряжения. Минус — намного меньшая емкость.
— Ток заряда Li-ion должен быть умеренным (0,5C для литий-иона на основе кобальта). Меньший зарядный ток сокращает время, в течение которого элемент находится при напряжении 4,20 В. Зарядка в 0,5C лишь незначительно увеличивает время зарядки по сравнению с 1C, потому что дозарядка будет короче. Зарядка с высоким током имеет тенденцию преждевременно подталкивать напряжение к пределу напряжения.
— Не разряжайте литий-ион слишком глубоко. Вместо этого заряжайте его часто. У литий-ионных нет проблем с памятью, как у никель-кадмиевых аккумуляторов. Для кондиционирования не требуются глубокие разряды.
Вместо этого заряжайте его часто. У литий-ионных нет проблем с памятью, как у никель-кадмиевых аккумуляторов. Для кондиционирования не требуются глубокие разряды.
— Не заряжайте литий-ионные аккумуляторы при температуре ниже нуля. Несмотря на прием заряда, произойдет необратимое покрытие металлическим литием, что ставит под угрозу безопасность батареи.
Мало того, что литий-ионный аккумулятор прослужит дольше благодаря более низкой скорости зарядки; умеренная скорость разряда также помогает. На рис. 5 показан срок службы в зависимости от скоростей заряда и разряда. Обратите внимание на улучшение лабораторных характеристик при скорости заряда и разряда 1C по сравнению с 2 и 3C.
| Рисунок 5: Срок службы литий-ионных аккумуляторов в зависимости от скорости заряда и разряда. Литий-кобальт обладает самой высокой плотностью энергии. Системы с марганцем и фосфатом гораздо более стабильны и обеспечивают более высокие токи нагрузки, чем системы с кобальтом.  |



 2012 авг; 32 (8): 1575-82. doi: 10.1016/j.wasman.2012.03.027. Epub 2012 23 апр.
Управление отходами. 2012.
PMID: 22534072
2012 авг; 32 (8): 1575-82. doi: 10.1016/j.wasman.2012.03.027. Epub 2012 23 апр.
Управление отходами. 2012.
PMID: 22534072 дои: 10.1177/0734242X19857130. Epub 2019 27 июня.
Управление отходами Res. 2019.
PMID: 31244410
Обзор.
дои: 10.1177/0734242X19857130. Epub 2019 27 июня.
Управление отходами Res. 2019.
PMID: 31244410
Обзор.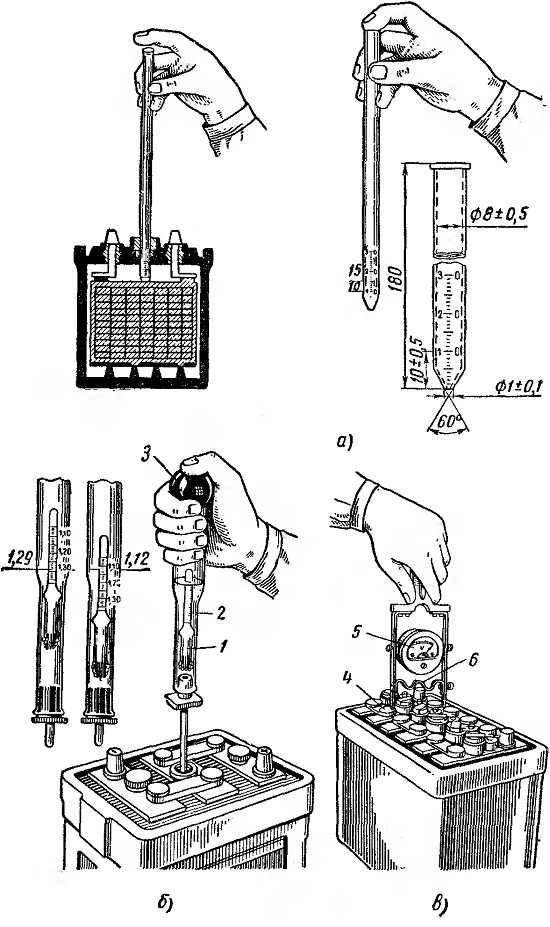 , Чжэн Л., Чжао З., Чжэнь А.Г.
Макваримба С.П. и соавт.
iНаука. 2022 28 апреля; 25 (5): 104321. doi: 10.1016/j.isci.2022.104321. Электронная коллекция 2022 20 мая.
iНаука. 2022.
PMID: 35602951
Бесплатная статья ЧВК.
Обзор.
, Чжэн Л., Чжао З., Чжэнь А.Г.
Макваримба С.П. и соавт.
iНаука. 2022 28 апреля; 25 (5): 104321. doi: 10.1016/j.isci.2022.104321. Электронная коллекция 2022 20 мая.
iНаука. 2022.
PMID: 35602951
Бесплатная статья ЧВК.
Обзор. Г., Торо Н., Гальегос С., Родригес М.Х.
Пинна Э.Г. и соавт.
Материалы (Базель). 2021 22 декабря; 15 (1): 44. дои: 10.3390/ma15010044.
Материалы (Базель). 2021.
PMID: 35009191
Бесплатная статья ЧВК.
Г., Торо Н., Гальегос С., Родригес М.Х.
Пинна Э.Г. и соавт.
Материалы (Базель). 2021 22 декабря; 15 (1): 44. дои: 10.3390/ma15010044.
Материалы (Базель). 2021.
PMID: 35009191
Бесплатная статья ЧВК.