Совет эксперта: как восстановить плотность аккумулятора? | Автобрюзгач
Источник: https://youtu.be/pJMbeqcrUg8Источник: https://youtu.be/pJMbeqcrUg8
Современный автомобильный аккумулятор представляет собой неразборное изделие, поэтому его обслуживание сводится к восстановлению заряда и контролю уровня и плотности электролита.
Рекомендуемая плотность раствора серной кислоты равна 1,28 грамм на см3 при комнатной температуре (допускаемое отклонение составляет 0,01). Аккумулятор при этом должен быть полностью заряжен – соотношение воды и серной кислоты в электролите напрямую зависит от степени его заряженности.
Это значение является оптимальным для умеренного климатического пояса. Электролит такой плотности не замерзает до –74С. Если же её увеличить до 1,35, то пластины АКБ подвергнутся ускоренной коррозии. При плотности 1,15 г/см3, как было экспериментально установлено, батарея уже перестаёт отдавать энергию, к тому же такой электролит замёрзнет уже при – 16С, что приведёт к разрушению корпуса аккумулятора и короблению пластин.
Для того, чтобы увеличить плотность электролита, потребуется добавление в него серной кислоты. Но постановлением правительства от 3.06. 2010 её продажа ограничена и подлежит контролю. В магазинах автозапчастей можно приобрести корректирующий электролит плотностью 1,4 г/см3. Добавляя его в «банки», можно увеличить концентрацию раствора.
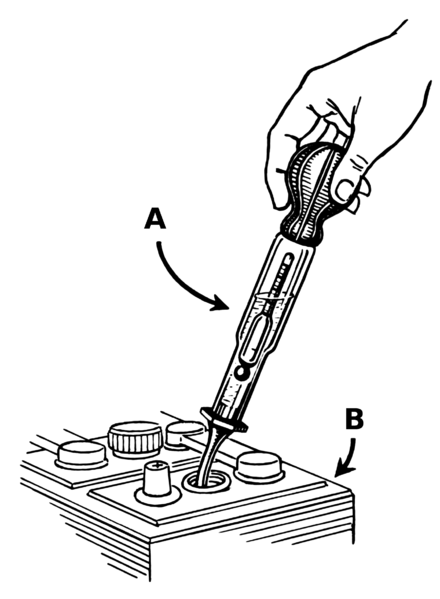
При этом учитывайте, что для равномерного распределения концентрированного раствора по объёму потребуется около получаса – иначе измерения плотности дадут некорректный результат. При необходимости повторяйте процедуру, откачивая электролит спринцовкой и добавляя корректирующий раствор. Контроль плотности осуществляется ареометром.
В тех же случаях, когда ареометра под рукой нет, а батарея подвела Вас при попытке запуска при первом похолодании, можно добавить электролит без измерения плотности, вернувшись к этому вопросу с наступлением тёплого времени года – чтобы избежать «съедания» пластин излишне концентрированным раствором.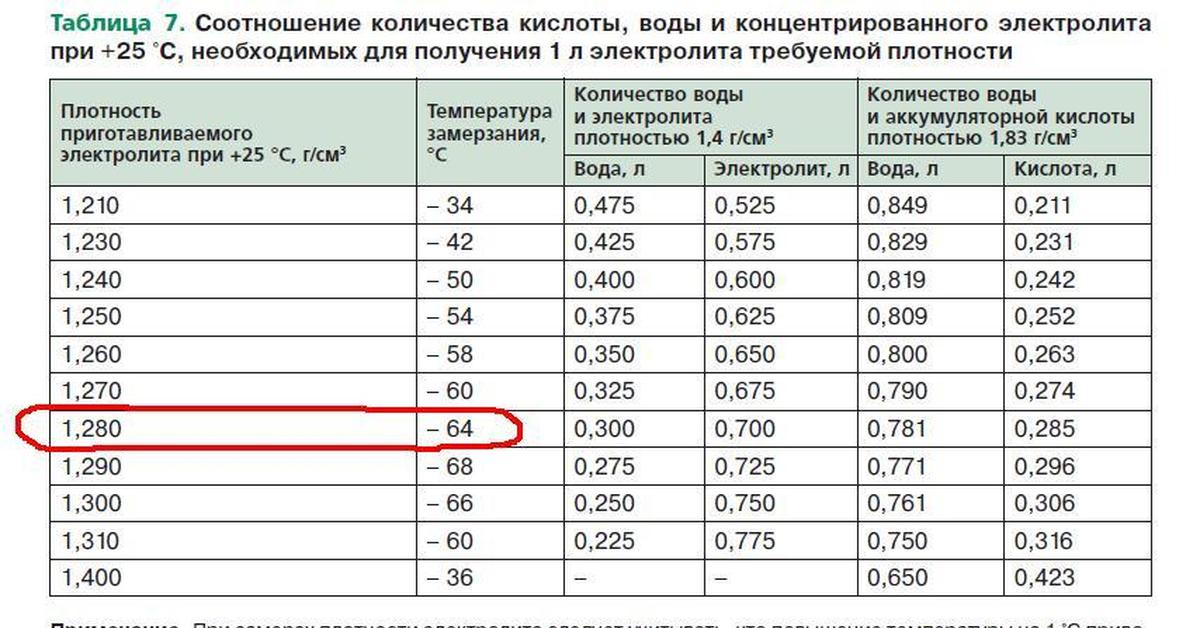
Полная же замена электролита потребует слива жидкости из батареи, для чего необходимо просверлить отверстия в нижней части каждой «банки», после чего потребуется восстанавливать герметичность корпуса. Но такой способ потребует навыков правильной пайки пластмассы и сопряжён с проблемами безопасной утилизации раствора серной кислоты.
Но в случае сульфатации пластин или замыкания «банок» восстановление и увеличение плотности электролита не будет способствовать возвращению батареи в строй – её можно будет лишь сдать с доплатой в обмен на новую.
Если вам понравилась статья, ставьте лайк и подписывайтесь на канал. Каждый день мы публикуем новые интересные статьи.
Защита АКБ в сильные морозы
Аккумулятор – сердце автомобиля! Именно от АКБ зависит запуск двигателя и функционирование всех приборов в салоне, поэтому важно правильно эксплуатировать и обслуживать батарею. Некоторые автолюбители считают, что, в зависимости от времени года, нужно уменьшать или увеличивать номинальную плотность электролита. Разберемся, так ли это.
Некоторые автолюбители считают, что, в зависимости от времени года, нужно уменьшать или увеличивать номинальную плотность электролита. Разберемся, так ли это.
Заводы-изготовители выпускают аккумуляторы с плотностью электролита в максимально заряженных АКБ: 1,27 – 1,28 г/см³. Для наших широт это оптимальная плотность, и регулировать ее не просто не рекомендуется, а даже запрещено. Плотность 1,27 г/см³ позволяет электролиту не замерзать до –60 °C. Конечно, если предстоит более суровая зима или требуется восстановить АКБ после сильной разрядки, плотность электролита увеличить придется, но не самостоятельно. Обратитесь к специалистам по обслуживанию автомобилей. Самостоятельно можно только корректировать уровень электролита дистиллированной водой, доливая до необходимого уровня. Увеличение номинальной плотности с помощью кислоты приводит к агрессивности среды, а, следовательно, к ускоренному осыпанию пластин аккумулятора.
Если в теплое время можно завести авто только с наполовину заряженным аккумулятором, то перед началом зимы заряда должно быть не менее 80%. Причина в том, что при минусовых температурах смазка в АКБ густеет, приводя к ее разрядке. В морозы требуется больше энергии на запуск холодного двигателя, интенсивную работу бортовой системы, печки, видеорегистратора, магнитолы, фар и т.д. Бросая автомобиль в ледяном гараже, во дворе, на стоянке, редко используя его из-за гололеда или снегопада, мы способствуем накапливанию разряженности АКБ, в результате чего снижается и плотность электролита. Ионы оседают на пластинах АКБ, а вода, входящая в его состав, кристаллизуется, расширяется и разрушает изоляторы между пластинами соседних банок. Таким образом, разряженный аккумулятор во время морозов приводит к замерзанию электролита и разрушению свинцовых пластин! Мутный электролит в банках – сигнал о гибели аккумулятора.
Зимой подзаряжайте АКБ хотя бы два раза в месяц, а размороженную «реанимируйте» малыми токами. Для этого можно использовать правило трех пятерок: при температуре -5 нужно поставить АКБ на зарядку током 5А на 5 часов.
Если нет возможности занести аккумулятор в дом, для восстановления энергетического баланса батареи необходимо не менее часа интенсивной поездки.
Для карбюраторных автомобилей – при оборотах не менее 1500 об/мин, для инжекторных – не менее 800-1000 об/мин. Электролиту нужно время, чтобы хорошо прогреться и зарядиться.
Перед тем как оставить автомобиль на несколько часов, убедитесь, что двери закрыты, а в салоне отключены все энергопотребляющие приборы.
 Не выключенные на ночь фары часто являются причиной разрядки аккумулятора.
Не выключенные на ночь фары часто являются причиной разрядки аккумулятора.Когда автомобиль предстоит оставить на морозе дольше 2 месяцев, обязательно проверьте все электрические системы машины на утечки, а лучше – снимите минусовую клемму. Снижение токов утечки до нуля оставят батарею заряженной на более долгий срок.
Потребитель должен следить за аккумулятором. Это прописано во всех гарантийных талонах, прилагаемых к АКБ. Заботьтесь о своем аккумуляторе, и он не подведет вас в дороге!
Как восстановить аккумулятор? — Автомобили
Посоветуйте пожалуйста хорошую литературу по обслуживанию или может быть статью/тему на форуме.
Уважаемый Андрей.
Вы сначала отрываете бабе руки-ноги, потом бьете ее топором по голове, а теперь спрашиваете как пришить все обратно и оживить бабу.
Аккумуляторы Варта нормально работают 5-6 лет но, после всех этих Ваших действий (заливка кислоты, езда с неизвестным реле-регулятором и т. п.) Вашему аккумулятору прямой путь на помойку. Но. Можно. Попробовать. оживить. Это займет много трудов и времени и результат не гарантируется.
Делаем следующее:
1. Полностью заряжаем аккумулятор током 10-часового режима заряда. для Вас это 62Ач/10 часов=6,2А. Признаки конца зарядки — бурное кипение электролита и напряжение аккумулятора не повышается в течение 0,5-1 часа.
2 Сливаем электролит из всех банок.
3. Покупаем в магазине дистиллированную воду и заливаем во все банки. Уровень воды на 5-10 мм выше верха пластин.
4. Ставим аккумулятор на зарядку током примерно 1А. Заряжаем до плотности электролита 1,06 (можно 1,1) г/см куб.
5. Когда плотность станет 1,06 1,1)- сливаем старую воду и заливаем чистую дистиллированную воду. Снова ставим на зарядку током 1А. Заряжаем до плотности 1,06 ( 1,1). Так несколько раз (3-4 раза, а может и больше), до тех пор, пока плотность не перестанет повышаться и напряжение аккумулятора при заряде будет постоянным в течение 2-5 часов.
6. Сливаем воду и покупаем чистый электролит плотностью 1,27-1,29. Заливаем во все банки.
7. Снова ставим аккумулятор на зарядку. Заряжаем током 0,1 емкости (6,2А) до бурного кипения электролита (газовыделения) и постоянства напряжения на зажимах аккумулятора.
8. Ставим аккумулятор на разрядку током 20 часового режима разряда — 62Ач / 20 часов =3,1А и засекаем время начала разрядки. Разряжаем до падения напряжения на аккумуляторе 10,8В. При разрядке стараемся поддерживать постоянство тока 3,1А и постоянно меряем напряжение.
После разрядки замеряем плотность тока по банкам. Разность в плотностях по банкам не более 0,01.
9. Если с плотностями и емкостью все в порядке, то после разряда не задерживаясь снова ставим на заряд током 0,1 емкости. Заряжаем около 10 — 12 часов. Признак конца заряда — бурное газовыделение и постоянство напряжения на клеммах аккумулятора в течение 0,5 часа. Плотность электролита в конце зарядки — 1,27-1,29. разность по банкам не более 0,01.
Не забывем при заряда следить за температурой аккумулятора. Она не должна подниматься выше 40град Цельсия.
10. Ставим аккумулятор на автомобиль, заводим, замеряем напряжение на его клеммах при работающем двигателе, должно быть выше 12,0В. Поднимаем обороты до 2200 — 2500 об/мин и на этих оборотах замеряем напряжение — должно быть не выше 1,4-14,8В — зависит от автомобиля.
Ну вот творите. Все займет 3-4 дня.
Как восстановить автомобильный аккумулятор
Не стоит сразу выбрасывать аккумулятор, если начал пропадать заряд или через раз прокручиваться стартер. Во многих случаях батарея подлежит ремонту. Зная, как восстановить автомобильный аккумулятор, можно продлить его эксплуатацию еще на несколько сезонов.
Дефекты аккумуляторной батареи
Неисправности батареи могут быть вызваны как внешними, так и внутренними причинами. К первым можно отнести:
- Повреждения (трещины) пластикового корпуса батареи вызванные внешними воздействиями либо процессами в самом аккумуляторе (перегрев, вздутие и пр.). При существенных повреждениях проведение ремонта нецелесообразно и лучше приобрести новую батарею. Незначительные повреждения можно устранить самостоятельно с помощью подручных инструментов и материалов, предварительно слив весь электролит. По окончании ремонтных работ следует залить свежий электролит и зарядить аккумулятор.

- Окисление контактных клемм. Ремонт сводится к зачистке окислов наждачной бумагой и ветошью или тряпкой. Нелишним будет зачистить контакты и на подключаемых кабелях. По окончании зачистки контакты и клеммы можно обработать небольшой порцией машинного масла.
Список внутренних неисправностей выглядит чуть внушительнее, причем некоторые из них вообще не позволяют восстановить аккумулятор:
- При неправильном использовании батареи, к примеру, глубоком разряде либо систематической недозарядке, могут повредиться элементы. А в случае нахождения разряженного аккумулятора на морозе замерзает электролит, что является причиной повреждения пластин или корпуса. Восстановление АКБ в таких случаях нецелесообразно.
- Осыпание угольных пластин диагностируется при потемнении электролита. Восстановление батареи в таком случае также нереально и следует приобрести новую.
- Сульфатация пластин является самой распространённой внутренней неисправностью аккумулятора.
 На ее начальной стадии батарея поддается восстановлению и чуть ниже будет указано, как это делается.
На ее начальной стадии батарея поддается восстановлению и чуть ниже будет указано, как это делается. - Замыкание пластин. Признаком этого дефекта является перегрев одной из банок и вскипание в ней электролита. В некоторых случаях спасением является замена свинцовых пластин, но нужно быть готовым и к полной замене батареи.
Методы восстановления
Сульфатация
Проявлением этого дефекта является белый налет крупнокристаллического сернокислого свинца на пластинах. Слой кристаллов прикрывает поры активного вещества, препятствуя прохождению электролита при зарядке батареи. Из-за этой неисправности резко возрастает сопротивление внутри аккумулятора с одновременным уменьшением его емкости. В результате батарея начинает стремительно заряжаться. Значения температуры электролита и напряжения также заметно растут, что влечет за собой резкое выделение газов. После установки в автомобиль такой аккумулятор чрезвычайно быстро разряжается.
Сульфатация пластин аккумулятора
Сульфатация может возникнуть из-за разряда батареи меньше 10,2 В, его продолжительного хранения в состоянии разряда, слишком низкого уровня электролита в банках, его малой плотности либо загрязнения сторонними примесями.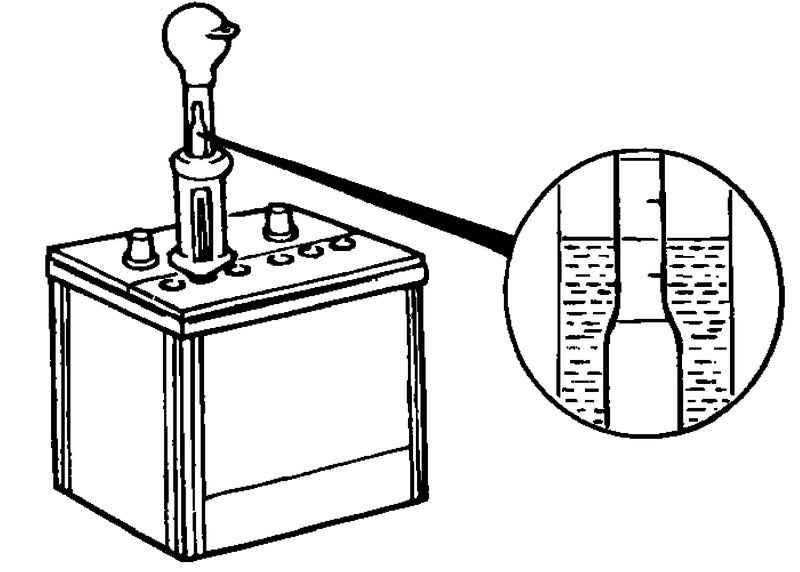
Аккумулятор поддается восстановлению только при незначительной сульфатации. Если процесс зашел далеко, то батарею придется менять. Процесс восстановления заключается в осуществлении нескольких циклов зарядки — разрядки батареи.
Сначала надо осуществить полный заряд АКБ и довести величину плотности электролита до значения 1,285 г/см3. Это можно сделать, вливая более плотный (1,4 г/см3) электролит.
Внимание! Ни в коем случае не доливать кислоту! Это только усугубит ситуацию.
Если возникнет необходимость в уменьшении плотности, то потребуется добавить дистиллированной воды.
После этого надо засечь время и разрядить батарею током около 0,5 А, используя лампу накаливания. Необходимо добиться снижения напряжения в каждой банке до 1,7 В либо до 10,2 В во всей батарее. Далее, используя величину разрядного тока и затраченного времени, следует определить реальную емкость аккумулятора. Если ее величина ниже номинальной, то процедуру заряда-разряда придется повторить. Практика показывает, что в большинстве случаев достаточно провести 3–4 цикла заряда-разряда. Добившись номинального значения емкости, можно считать аккумулятор восстановленным, поставить его на зарядку и, по ее окончании, эксплуатировать в обычном режиме.
Практика показывает, что в большинстве случаев достаточно провести 3–4 цикла заряда-разряда. Добившись номинального значения емкости, можно считать аккумулятор восстановленным, поставить его на зарядку и, по ее окончании, эксплуатировать в обычном режиме.
Короткое замыкание
Этот дефект может возникнуть при неисправности сепараторов либо короблении пластин в процессе разрядки высокоамперным током (продолжительное пользование стартером, либо проба на искру). Сквозь появившиеся на пластине трещины начинает проникать активное вещество. Соскальзывая вниз, оно заполняет внутреннее пространство и соединяет разнополюсные пластины. Величина тока разряда резко увеличивается, что приводит к выходу АКБ из строя.
Повреждение сепараторов пластин аккумулятора
Устранение неисправности состоит в добавлении в электролит особой десульфатизирующей присадки. Предварительно его плотность надо довести до 1,28 г/см3. Получившуюся смесь для полного растворения следует оставить на 48 часов, а затем залить в батарею и снова измерить величину плотности.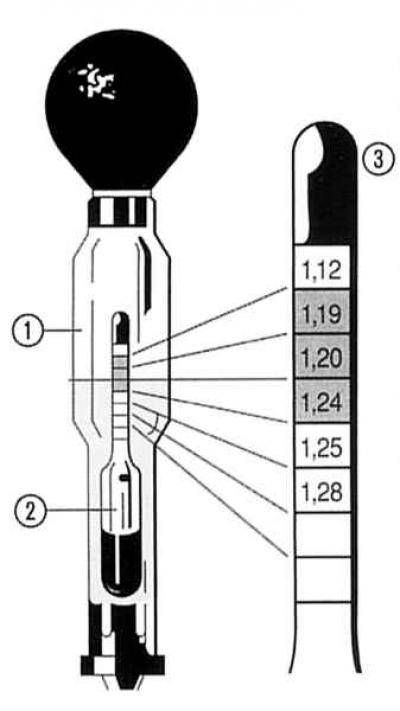
Если ее величина заметно не изменилась, то можно приступить к процессу зарядки — разрядки, который следует повторить несколько раз. Если в процессе зарядки батарея не греется, а электролит не вскипает, то силу тока можно наполовину снизить. Если спустя два часа значение плотности не изменилось, то зарядку можно прекратить.
При заметном изменении значения плотности больше 1,28 г/см3 в электролит необходимо долить воду, а при отклонении в меньшую сторону — серную кислоту. Доведя величину плотности до номинального уровня, можно повторить процесс зарядки.
Также бывают случаи когда грязь, жир и влага создают токопроводящий слой, который медленно будет убивать ваш аккумулятор, а зимой разрядить под «ноль». Это явление достаточно редкое и механик может о нём не знать или попросту упустить, что в итоге приведёт к ошибочной рекомендации о замене батареи. Утечку легко проверить самому при помощи мультиметра, исключив преждевременные траты.
Утечка по корпусу аккумуляятора
Обратная зарядка
Процесс заключается в изменении полярности аккумулятора. Перед тем как восстановить автомобильный аккумулятор этим способом, надо подыскать мощный источник напряжения не менее 20 В и тока не менее 80 А. Вполне подойдет сварочный аппарат.
Перед тем как восстановить автомобильный аккумулятор этим способом, надо подыскать мощный источник напряжения не менее 20 В и тока не менее 80 А. Вполне подойдет сварочный аппарат.
Для начала следует открыть пробки банок и подсоединить «плюс» источника напряжения к «минусу» батареи, а «минус» источника к ее «плюсу». Затем можно приступать к процессу зарядки в течение получаса. Электролит при этом будет бурно кипеть. По окончании зарядки следует выключить оборудование, слить электролит, промыть аккумулятор горячей водой и залить свежий электролит.
После этого с помощью обычного 10–15 амперного зарядного устройства следует зарядить АКБ в течение суток. При этом следует помнить, что полярность батареи уже изменилась.
После выполнения этого процесса аккумулятор при правильной эксплуатации может прослужить еще несколько лет.
Необслуживаемые АКБ
Практически на все новые модели автомобилей устанавливаются так называемые необслуживаемые аккумуляторы, которые по замыслу производителей не должны отвлекать на себя внимание. Однако их эксплуатация и зарядка отличается некоторыми нюансами.
Однако их эксплуатация и зарядка отличается некоторыми нюансами.
Прежде всего, следует помнить о том, что в теплый сезон такие батареи подзаряжаются в машине постоянно. Но их зарядка с помощью специального устройства является более щадящей и правильной, чем постоянная подпитка от автогенератора.
Ситуация существенно меняется с приходом зимы. В мороз смазка в двигателе густеет и для его запуска требуется подача стартового тока большей величины. Это может привести к быстрому разряду аккумулятора. Поэтому зарядка необслуживаемой батареи зимой является насущной необходимостью.
Этот процесс надо осуществлять очень осторожно, так как определить в ней величину плотности электролита невозможно. Полагаться можно только на значение остаточного напряжения и делать выводы из сложившейся ситуации.
Частично заряженную батарею следует непрерывно заряжать около трех часов подачей напряжения 14–14,5 В, контролируя только значение силы тока — от 25 А в самом начале процесса до 0,20 А при полном заряде.
Для полностью разряженной батареи цикл зарядки должен длиться не менее суток и осуществляться с максимумом внимания. Регулятор напряжения необходимо выставить на значение, численно равное десяти процентам от емкости заряжаемой АКБ в ампер-часах. При первых признаках активного образования газов процесс следует прекратить. По завершении зарядки обязательно надо проверить величину напряжения на соответствие номинальному значению.
Окисление клемм
Для предотвращения большинства неполадок автомобильного аккумулятора достаточно периодически очищать контактные клеммы и выводы, а также раз в полгода осуществлять его полную зарядку с использованием стационарного устройства. А регулярный уход за вращающимися и трущимися деталями двигателя и стартера позволит продлить срок службы батареи не менее, чем до 5 лет.
24 ноября 2011
Аккумулятор — это маленькое сердце мотора и его бесперебойная работа жизненно необходима для запуска.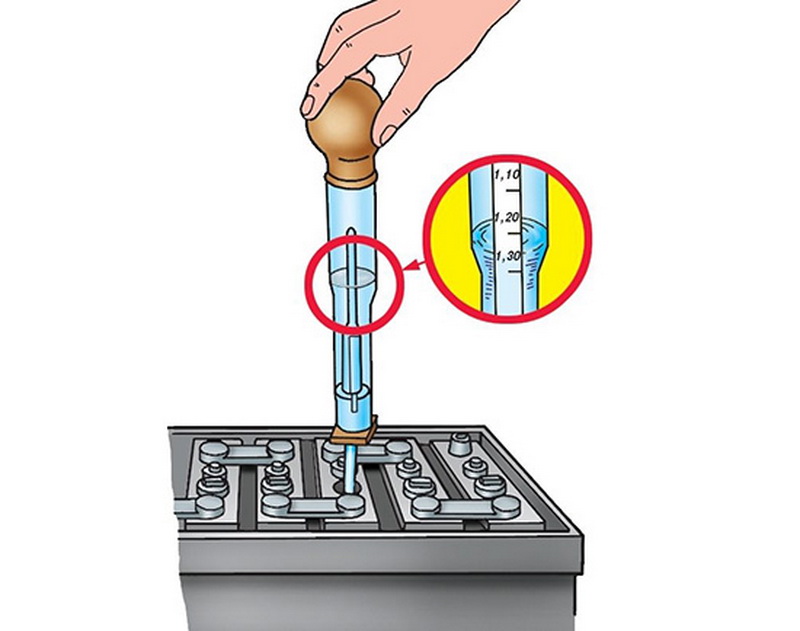
двигателя. Многим автомобилистам знакома ситуация, когда машина неожиданно перестает заводиться или на некоторых автомобилях при разряженной батарее в нее просто не попасть, так как машина не открывается. Приходится вызывать мастера по вскрытию автомобиля, ждать его приезда. День полностью летит под откос, все планы рушатся. Поэтому очень важно правильно эксплуатировать АКБ, а в случае необходимости, вовремя заменить.
Так что же влияет на продолжительность жизни аккумулятора?
Одной из причин, по которой аккумулятор выходит из строя, является температурные условия окружающей среды. Низкие и высокие температуры снижают срок службы батареи.
У большинства автомобилей аккумулятор находится по соседству с двигателем, который нагревает его, что снижает срок службы в несколько раз. Фирмы Audi, BMW, Jaguar и Rolls-Royse убрали аккумулятор из двигательного отсека, а недостатки наличия дополнительного провода уравновесились повышенной надежностью батареи.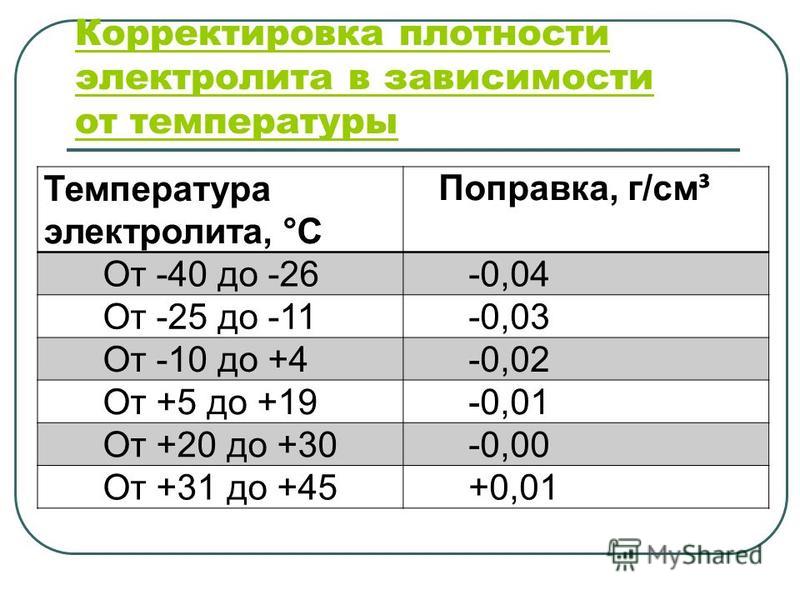 В моделях класса «супермини» аккумуляторы всегда находились в багажнике.
В моделях класса «супермини» аккумуляторы всегда находились в багажнике.
Есть и другие решения. Например, в новой модели Peugeot 406 устанавливается аккумулятор с двойным корпусом. Между стенками прогоняется воздух, что предохраняет батарею от перегрева. Но не все являются счастливыми обладателями машины, у которой конструктивно аккумулятор защищен от перегрева. Поэтому не удивляйтесь, если после жаркого лета аккумулятор внезапно «умирает».
В зимнее время важно контролировать уровень заряда в аккумуляторе. При разряде АКБ снижается плотность электролита, то есть уменьшается удельное количество серной кислоты, содержащейся в растворе электролита, и образуется вода. При плотности 1,11 г/см3 электролит замерзнет уже при -7 0С, а при плотности 1,27 г/см3 – только при -58 0С.
Плотность электролита у исправной полностью заряженной АКБ для условий центральных районов страны должна быть 1,27 ÷1,28г/см3 при +25С и нормальном уровне над блоками пластин. В южных районах страны значение плотности электролита 1,24 ÷1,25г/см3 . В районах Сибири плотность электролита в АКБ на зимний период устанавливают 1,30г/см3 (чтобы частично разряженная АКБ при минус 40 ÷45С не разрушалась льдом), а на летний период плотность снижают, чтобы уменьшить разрушение пластин в этот период от высокой плотности электролита.
В районах Сибири плотность электролита в АКБ на зимний период устанавливают 1,30г/см3 (чтобы частично разряженная АКБ при минус 40 ÷45С не разрушалась льдом), а на летний период плотность снижают, чтобы уменьшить разрушение пластин в этот период от высокой плотности электролита.
Если батарею в разряженном состоянии оставить на морозе , то образовавшаяся вода замерзнет, расширится и деформирует корпус. Такой аккумулятор восстановлению не подлежит. Если вам повезло, и батарея замерзла не на весь объем,обошлось без деформации корпуса, то ее можно восстановить. Лед должен полностью растаять при комнатной температуре, и только потом следует зарядить АКБ.
Если при запуске двигателя в зимнее время аккумулятор разрядился в «ноль», какие действия нужно предпринять? Глубокий разряд вреден для любой батареи. Если это произошло, то необходимо зарядить аккумулятор от стационарного зарядного устройства, но не позднее чем через 2-3 дня после глубокого разряда батареи.
Еще одной причиной быстрого износа аккумулятора является режим эксплуатации автомобиля. Многочасовое простаивание в пробках приводит к тому, что генератор не может обеспечить энергией все энергопотребители в машине. Дополнительным источником энергии становится аккумулятор.За 45 минут такой работы средний АКБ может истощиться настолько, что повторный запуск выключенного двигателя окажется уже невозможным. Для восстановления потребуется не меньше 30 минут нормальной езды, прежде чем можно будет снова остановиться. Такие глубокие разряды ведут к сульфатации аккумулятора и уменьшении его емкости (емкость аккумулятора прямо пропорциональна площади поверхности пластин, покрытой активными веществами. У засульфатированного аккумулятора, часть активных веществ связана в сульфате свинца, а часть поверхности пластин покрыта не активными веществами, а сульфатом. Поэтому при разряде засульфатированный аккумулятор отдает меньшую емкость, чем аккумулятор в нормальном состоянии). К сожалению, пробки не исчезают с дорог мегаполиса. Поэтому рекомендуется ставить на машину аккумулятор, максимальный по емкости и пусковым токам .
Многочасовое простаивание в пробках приводит к тому, что генератор не может обеспечить энергией все энергопотребители в машине. Дополнительным источником энергии становится аккумулятор.За 45 минут такой работы средний АКБ может истощиться настолько, что повторный запуск выключенного двигателя окажется уже невозможным. Для восстановления потребуется не меньше 30 минут нормальной езды, прежде чем можно будет снова остановиться. Такие глубокие разряды ведут к сульфатации аккумулятора и уменьшении его емкости (емкость аккумулятора прямо пропорциональна площади поверхности пластин, покрытой активными веществами. У засульфатированного аккумулятора, часть активных веществ связана в сульфате свинца, а часть поверхности пластин покрыта не активными веществами, а сульфатом. Поэтому при разряде засульфатированный аккумулятор отдает меньшую емкость, чем аккумулятор в нормальном состоянии). К сожалению, пробки не исчезают с дорог мегаполиса. Поэтому рекомендуется ставить на машину аккумулятор, максимальный по емкости и пусковым токам . Можно ли устанавливать батарею большей емкости, чем рекомендована заводом изготовителем автомобиля? Можно, если в этом есть необходимость, например, установлено дополнительное электрооборудование, или автомобиль эксплуатируется в условиях экстремально низких температур. Даже скромный двухканальный усилитель мощности потребляет приличное количество энергии – уже после 15-минутной демонстрации возможностей аудиосистемы вольтметр высвечивает под нагрузкой жалкие 11,4 В вместо привычных 12,5 В! Словом, любители мощных аудиоустановок, имейте в виду – иногда инсталляторы умалчивают о том, откуда брать запас электроэнергии для «дракона» — усилителя, этот вопрос решается только одним путем – заменой генератора более мощным и установкой пары АКБ. Аккумулятор должен подходить по габаритам.
Можно ли устанавливать батарею большей емкости, чем рекомендована заводом изготовителем автомобиля? Можно, если в этом есть необходимость, например, установлено дополнительное электрооборудование, или автомобиль эксплуатируется в условиях экстремально низких температур. Даже скромный двухканальный усилитель мощности потребляет приличное количество энергии – уже после 15-минутной демонстрации возможностей аудиосистемы вольтметр высвечивает под нагрузкой жалкие 11,4 В вместо привычных 12,5 В! Словом, любители мощных аудиоустановок, имейте в виду – иногда инсталляторы умалчивают о том, откуда брать запас электроэнергии для «дракона» — усилителя, этот вопрос решается только одним путем – заменой генератора более мощным и установкой пары АКБ. Аккумулятор должен подходить по габаритам.
Еще одним не маловажным фактором, влияющим на срок службы аккумулятора, является интенсивность его эксплуатации. Жизнь аккумулятора измеряется в циклах. Один цикл – это «заряд-разряд».Увеличивая количество циклов, мы уменьшаем срок службы АКБ. Не используйте АКБ для сторонних энергопотребителей, например, на природе, на даче и.т.д. Без специального оборудования невозможно определить степень заряда батареи и просчитать динамику разрядки, а значит, велика вероятность глубокого разряда. Используйте для этих целей резервный аккумулятор. Тоже самое относится и к «прикуриванию» другого автомобиля. Это можно делать при соблюдении определенных требований. Двигатель автомобиля, от которого осуществляют «прикуривание», должен быть обязательно выключен. При этом надо помнить, что нельзя прикуривать автомобиль у которого емкость аккумулятора больше вашего.
Не используйте АКБ для сторонних энергопотребителей, например, на природе, на даче и.т.д. Без специального оборудования невозможно определить степень заряда батареи и просчитать динамику разрядки, а значит, велика вероятность глубокого разряда. Используйте для этих целей резервный аккумулятор. Тоже самое относится и к «прикуриванию» другого автомобиля. Это можно делать при соблюдении определенных требований. Двигатель автомобиля, от которого осуществляют «прикуривание», должен быть обязательно выключен. При этом надо помнить, что нельзя прикуривать автомобиль у которого емкость аккумулятора больше вашего.
Так же на срок службы аккумулятора влияет исправность электрооборудования в автомобиле. Не правильно установленное оборудование ведет к утечке тока. Как правило , она начинает себя проявлять в полную силу зимой, поскольку аккумулятор уже не может при низкой температуре долгое время держать номинальную емкость. Если в автомобиле не работает генератор, то все энергопотребители питаются от аккумулятора, что ведет к его глубокому разряду , а в дальнейшем , к выходу из строя.
« все статьи
Батарея и производительность iPhone — Служба поддержки Apple (KW)
При низком уровне заряда батареи, более высоком химическом возрасте или более низких температурах пользователи с большей вероятностью могут столкнуться с неожиданными отключениями. В крайних случаях отключения могут происходить чаще, что делает устройство ненадежным или непригодным для использования. Для iPhone 6, iPhone 6 Plus, iPhone 6s, iPhone 6s Plus, iPhone SE (1-го поколения), iPhone 7 и iPhone 7 Plus iOS динамически управляет пиками производительности, чтобы предотвратить неожиданное отключение устройства, чтобы iPhone по-прежнему мог работать. использовал.Эта функция управления производительностью предназначена только для iPhone и не применяется ни к каким другим продуктам Apple. Начиная с iOS 12.1, iPhone 8, iPhone 8 Plus и iPhone X включают эту функцию; iPhone XS, iPhone XS Max и iPhone XR включают эту функцию, начиная с iOS 13.1. Влияние управления производительностью на эти более новые модели может быть менее заметным из-за их более совершенного аппаратного и программного обеспечения.
Это управление производительностью основано на сочетании температуры устройства, уровня заряда аккумулятора и импеданса аккумулятора.Только если этого требуют эти переменные, iOS будет динамически управлять максимальной производительностью некоторых системных компонентов, таких как ЦП и ГП, чтобы предотвратить неожиданное завершение работы. В результате рабочие нагрузки устройств будут автоматически балансироваться, что позволит более плавно распределять системные задачи, а не сразу увеличивать производительность. В некоторых случаях пользователь может не заметить каких-либо различий в ежедневной работе устройства. Уровень воспринимаемых изменений зависит от того, насколько управление производительностью требуется для конкретного устройства.
В случаях, когда требуются более экстремальные формы управления производительностью, пользователь может заметить такие эффекты, как:
- Увеличение времени запуска приложения
- Более низкая частота кадров при прокрутке
- Затемнение подсветки (которое можно переопределить в Центре управления)
- Уменьшить громкость динамика до -3 дБ
- Постепенное снижение частоты кадров в некоторых приложениях
- В самых крайних случаях вспышка камеры будет отключена, как видно в пользовательском интерфейсе камеры
- Приложения, обновляющиеся в фоновом режиме, могут потребовать перезагрузки при запуске
Эта функция управления производительностью не влияет на многие ключевые области. Некоторые из них включают:
Некоторые из них включают:
- Качество сотовой связи и пропускная способность сети
- Качество захваченных фото и видео
- Производительность GPS
- Точность определения местоположения
- Датчики, такие как гироскоп, акселерометр, барометр
- Apple Pay
При низком уровне заряда батареи и более низких температурах изменения в управлении производительностью носят временный характер. Если аккумулятор устройства химически устарел, изменения в управлении производительностью могут быть более продолжительными.Это связано с тем, что все перезаряжаемые батареи являются расходными материалами и имеют ограниченный срок службы, который в конечном итоге необходимо заменить. Если это повлияло на вас и вы хотите улучшить производительность вашего устройства, замена аккумулятора устройства может помочь.
островков неактивного лития ползут, как черви, чтобы снова соединиться со своими электродами, восстанавливая емкость и срок службы батареи — ScienceDaily
Исследователи из Национальной ускорительной лаборатории SLAC Министерства энергетики и Стэнфордского университета, возможно, нашли способ оживить перезаряжаемые литиевые батареи, потенциально увеличение ассортимента электромобилей и увеличение времени автономной работы электронных устройств нового поколения.
По мере цикла литиевых батарей в них накапливаются небольшие островки неактивного лития, которые отрезаны от электродов, что снижает способность батареи накапливать заряд. Но исследовательская группа обнаружила, что они могут заставить этот «мертвый» литий ползти, как червяк, к одному из электродов, пока он снова не соединится, частично обратив нежелательный процесс вспять.
Добавление этого дополнительного шага замедлило износ их тестовой батареи и увеличило срок ее службы почти на 30%.
«В настоящее время мы изучаем возможность восстановления потерянной емкости литий-ионных аккумуляторов с помощью чрезвычайно быстрой стадии разрядки», — сказал постдокторант Стэнфордского университета Фан Лю, ведущий автор исследования, опубликованного в декабре 2019 года.22 в Природа .
Потеря связи
Большое количество исследований направлено на поиск способов изготовления перезаряжаемых аккумуляторов с меньшим весом, более длительным сроком службы, повышенной безопасностью и более высокой скоростью зарядки, чем литий-ионная технология, используемая в настоящее время в мобильных телефонах, ноутбуках и электромобилях. Особое внимание уделяется разработке литий-металлических батарей, которые могут хранить больше энергии на единицу объема или веса. Например, в электромобилях эти батареи следующего поколения могут увеличить пробег на одном заряде и, возможно, занимать меньше места в багажнике.
Особое внимание уделяется разработке литий-металлических батарей, которые могут хранить больше энергии на единицу объема или веса. Например, в электромобилях эти батареи следующего поколения могут увеличить пробег на одном заряде и, возможно, занимать меньше места в багажнике.
Оба типа батарей используют положительно заряженные ионы лития, которые перемещаются между электродами. Со временем часть металлического лития становится электрохимически неактивной, образуя изолированные островки лития, которые больше не соединяются с электродами. Это приводит к потере емкости и представляет собой особую проблему для литий-металлических технологий и для быстрой зарядки литий-ионных аккумуляторов.
Однако в новом исследовании исследователи продемонстрировали, что они могут мобилизовать и восстановить изолированный литий, чтобы продлить срок службы батареи.
«Я всегда думал, что изолированный литий — это плохо, так как он вызывает разложение батарей и даже возгорание», — сказал Йи Цуй, профессор Стэнфордского университета и SLAC и исследователь Стэнфордского института исследований материалов и энергии (SIMES), возглавлявший исследование. «Но мы обнаружили, как электрически воссоединить этот «мертвый» литий с отрицательным электродом, чтобы реактивировать его».
«Но мы обнаружили, как электрически воссоединить этот «мертвый» литий с отрицательным электродом, чтобы реактивировать его».
Ползучие, не мертвые
Идея исследования родилась, когда Цуй предположил, что приложение напряжения к катоду и аноду батареи может заставить изолированный островок лития физически перемещаться между электродами — процесс, который его команда подтвердила своими экспериментами.
Ученые изготовили оптическую ячейку с катодом из литий-никеля-марганца-оксида кобальта (NMC), литиевым анодом и изолированным островком лития между ними. Это тестовое устройство позволило им отслеживать в режиме реального времени, что происходит внутри батареи во время ее использования.
Они обнаружили, что изолированный литиевый остров вовсе не был «мертвым», а реагировал на работу батареи. При зарядке элемента островок медленно приближался к катоду; при разрядке он полз в обратную сторону.
«Это похоже на очень медленного червя, который выдвигает голову вперед и втягивает хвост, чтобы двигаться нанометр за нанометром», — сказал Цуй.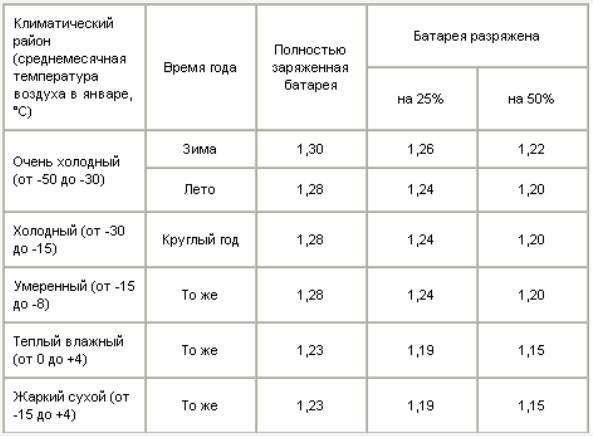 «В этом случае он перемещается, растворяясь на одном конце и откладывая материал на другом конце. Если мы сможем поддерживать движение литиевого червя, он в конечном итоге коснется анода и восстановит электрическое соединение».
«В этом случае он перемещается, растворяясь на одном конце и откладывая материал на другом конце. Если мы сможем поддерживать движение литиевого червя, он в конечном итоге коснется анода и восстановит электрическое соединение».
Увеличение срока службы
Результаты, подтвержденные учеными с помощью других тестовых аккумуляторов и с помощью компьютерного моделирования, также демонстрируют, как изолированный литий может быть восстановлен в реальном аккумуляторе путем изменения протокола зарядки.
«Мы обнаружили, что можем перемещать отделенный литий к аноду во время разряда, и эти движения происходят быстрее при более высоких токах», — сказал Лю. «Поэтому мы добавили быстрый этап сильноточной разрядки сразу после зарядки аккумулятора, который переместил изолированный литий достаточно далеко, чтобы снова соединить его с анодом. Это повторно активирует литий, чтобы он мог участвовать в сроке службы аккумулятора».
Она добавила: «Наши результаты также имеют большое значение для проектирования и разработки более надежных литий-металлических батарей. »
»
Эта работа финансировалась Управлением по энергоэффективности и возобновляемым источникам энергии Министерства энергетики США, Управлением транспортных технологий в рамках программ исследования аккумуляторных материалов (BMR), консорциума Battery 500 и программы eXtreme Fast Charge Cell Evaluation of Li-ion аккумуляторов (XCEL).
Аккумуляторы для гибридных и сменных электромобилей
В большинстве подключаемых гибридов и полностью электрических транспортных средств используются подобные литий-ионные аккумуляторы.
Системы накопления энергии, обычно батареи, необходимы для гибридных электромобилей (HEV), подключаемых гибридных электромобилей (PHEV) и полностью электрических транспортных средств (EV).
Типы систем накопления энергии
Следующие системы накопления энергии используются в HEV, PHEV и EV.
Литий-ионные батареи
Литий-ионные аккумуляторы в настоящее время используются в большинстве портативных устройств бытовой электроники, таких как сотовые телефоны и ноутбуки, из-за их высокой энергии на единицу массы по сравнению с другими системами хранения электроэнергии. Они также имеют высокое отношение мощности к весу, высокую энергоэффективность, хорошие характеристики при высоких температурах и низкий саморазряд.Большинство компонентов литий-ионных аккумуляторов могут быть переработаны, но стоимость восстановления материалов остается проблемой для отрасли. Министерство энергетики США также поддерживает Премию по переработке литий-ионных аккумуляторов для определения решений по сбору, сортировке, хранению и транспортировке отработанных и выброшенных литий-ионных аккумуляторов для возможной переработки и восстановления материалов. В большинстве современных PHEV и электромобилей используются литий-ионные аккумуляторы, хотя точный химический состав часто отличается от химического состава аккумуляторов бытовой электроники.Продолжаются исследования и разработки, направленные на снижение их относительно высокой стоимости, продление срока их службы и решение проблем безопасности в отношении перегрева.
Они также имеют высокое отношение мощности к весу, высокую энергоэффективность, хорошие характеристики при высоких температурах и низкий саморазряд.Большинство компонентов литий-ионных аккумуляторов могут быть переработаны, но стоимость восстановления материалов остается проблемой для отрасли. Министерство энергетики США также поддерживает Премию по переработке литий-ионных аккумуляторов для определения решений по сбору, сортировке, хранению и транспортировке отработанных и выброшенных литий-ионных аккумуляторов для возможной переработки и восстановления материалов. В большинстве современных PHEV и электромобилей используются литий-ионные аккумуляторы, хотя точный химический состав часто отличается от химического состава аккумуляторов бытовой электроники.Продолжаются исследования и разработки, направленные на снижение их относительно высокой стоимости, продление срока их службы и решение проблем безопасности в отношении перегрева.
Никель-металлогидридные батареи
Никель-металлогидридные батареи, обычно используемые в компьютерном и медицинском оборудовании, обладают разумной удельной энергией и удельной мощностью. Никель-металлогидридные батареи имеют гораздо более длительный жизненный цикл, чем свинцово-кислотные батареи, они безопасны и устойчивы к небрежному обращению. Эти батареи широко используются в HEV.Основными проблемами, связанными с никель-металлгидридными батареями, являются их высокая стоимость, высокий саморазряд и выделение тепла при высоких температурах, а также необходимость контроля потерь водорода.
Никель-металлогидридные батареи имеют гораздо более длительный жизненный цикл, чем свинцово-кислотные батареи, они безопасны и устойчивы к небрежному обращению. Эти батареи широко используются в HEV.Основными проблемами, связанными с никель-металлгидридными батареями, являются их высокая стоимость, высокий саморазряд и выделение тепла при высоких температурах, а также необходимость контроля потерь водорода.
Свинцово-кислотные аккумуляторы
Свинцово-кислотные аккумуляторы могут иметь высокую мощность, быть недорогими, безопасными и надежными. Однако низкая удельная энергия, плохие характеристики при низких температурах и короткий календарный и циклический срок службы препятствуют их использованию. Разрабатываются усовершенствованные свинцово-кислотные аккумуляторы большой мощности, но эти аккумуляторы используются только в имеющихся в продаже электромобилях для вспомогательных нагрузок.
Ультраконденсаторы
Ультраконденсаторы накапливают энергию в поляризованной жидкости между электродом и электролитом. Емкость накопления энергии увеличивается по мере увеличения площади поверхности жидкости. Ультраконденсаторы могут обеспечивать транспортным средствам дополнительную мощность при ускорении и подъеме на холм, а также помогают восстанавливать энергию торможения. Они также могут быть полезны в качестве вторичных накопителей энергии в транспортных средствах с электроприводом, поскольку они помогают электрохимическим батареям выравнивать мощность нагрузки.
Емкость накопления энергии увеличивается по мере увеличения площади поверхности жидкости. Ультраконденсаторы могут обеспечивать транспортным средствам дополнительную мощность при ускорении и подъеме на холм, а также помогают восстанавливать энергию торможения. Они также могут быть полезны в качестве вторичных накопителей энергии в транспортных средствах с электроприводом, поскольку они помогают электрохимическим батареям выравнивать мощность нагрузки.
Переработка батарей
Транспортные средства с электроприводом появились в США относительно недавно.S. автомобильный рынок, поэтому только небольшое количество из них подошло к концу срока службы. В результате доступно несколько бывших в употреблении аккумуляторов от электромобилей, что ограничивает масштабы инфраструктуры по переработке аккумуляторов. Поскольку автомобили с электроприводом становятся все более распространенными, рынок переработки аккумуляторов может расшириться.
Широко распространенная переработка аккумуляторов предотвратит попадание опасных материалов в поток отходов как в конце срока службы аккумулятора, так и в процессе его производства. В настоящее время ведется работа по разработке процессов переработки аккумуляторов, которые сводят к минимуму воздействие на жизненный цикл использования литий-ионных и других типов аккумуляторов в транспортных средствах. Но не все процессы переработки одинаковы:
В настоящее время ведется работа по разработке процессов переработки аккумуляторов, которые сводят к минимуму воздействие на жизненный цикл использования литий-ионных и других типов аккумуляторов в транспортных средствах. Но не все процессы переработки одинаковы:
- Плавка : Процессы плавки извлекают основные элементы или соли. Эти процессы сейчас работают в больших масштабах и могут работать с несколькими типами батарей, включая литий-ионные и никель-металлгидридные. Плавление происходит при высоких температурах, а органические материалы, включая электролит и угольные аноды, сжигаются в качестве топлива или восстановителя.Ценные металлы извлекаются и отправляются на аффинаж, чтобы продукт был пригоден для любого использования. Другие материалы, в том числе литий, содержатся в шлаке, который теперь используется в качестве добавки к бетону.
- Прямое восстановление : С другой стороны, некоторые процессы переработки напрямую восстанавливают материалы, пригодные для использования в батареях.
 Компоненты разделяются различными физическими и химическими процессами, и все активные материалы и металлы могут быть восстановлены. Прямое восстановление представляет собой низкотемпературный процесс с минимальным потреблением энергии.
Компоненты разделяются различными физическими и химическими процессами, и все активные материалы и металлы могут быть восстановлены. Прямое восстановление представляет собой низкотемпературный процесс с минимальным потреблением энергии. - Промежуточные процессы : Третий тип процесса находится между двумя крайностями. В таких процессах могут использоваться несколько типов батарей, в отличие от прямого восстановления, но материалы извлекаются дальше по производственной цепочке, чем при плавке.
Разделение различных материалов для аккумуляторов часто является камнем преткновения при восстановлении ценных материалов. Таким образом, конструкция батареи, предусматривающая разборку и переработку, важна для успеха электромобилей с точки зрения устойчивости.Стандартизация батарей, материалов и конструкции элементов также упростит и удешевит переработку.
См. отчет: Техническая и экономическая целесообразность использования бывших в употреблении аккумуляторов для электромобилей в стационарных устройствах.
Дополнительная информация
Узнайте больше об исследованиях и разработках аккумуляторов на страницах хранения энергии Национальной лаборатории возобновляемых источников энергии и на странице аккумуляторов Управления автомобильных технологий Министерства энергетики США.
Ремонт и техническое обслуживание аккумуляторов | Energic Plus
Что означает восстановление батареи и почему это полезно?
Сульфатированию в основном подвержены свинцово-кислотные аккумуляторы.Это явление возникает, когда батарея полностью разряжена, но возвращается к нормальному состоянию, когда вы перезаряжаете батарею. Однако естественные процессы не эффективны на 100 %. Сульфатные части прикрепляются к пластинам, влияя на общую емкость аккумулятора. Для зарядки требуется больше энергии, и температура батареи повышается, что сокращает срок службы батареи. Это результат того, что технология зарядки не совсем эффективна.
Восстановление аккумулятора или последующая процедура могут восстановить или продлить срок службы аккумулятора. Предыдущий анализ предоставляет информацию о состоянии батареи и позволяет нам диагностировать, возможно ли восстановить батарею. Данная услуга позволит дольше прослужить аккумулятору, что будет финансово выгодно работодателю.
Предыдущий анализ предоставляет информацию о состоянии батареи и позволяет нам диагностировать, возможно ли восстановить батарею. Данная услуга позволит дольше прослужить аккумулятору, что будет финансово выгодно работодателю.
У нас есть инструменты для подъема аккумуляторных вилочных погрузчиков, машин для гольфа, лодок, поездов, телекоммуникационных компаний, распределительных компаний, предприятий по производству электроэнергии и т. д. Наше устройство для восстановления аккумуляторов удаляет сульфат свинца с помощью процесса электрических высокочастотных пульсаций.
Восстановление батареи также называется регенерацией батареи или десульфатацией батареи .
Нажмите здесь, чтобы получить дополнительную информацию о нашем решении для восстановления аккумуляторов и нашем регенераторе аккумуляторов.
Как работает восстановление батареи?
1) Ежегодное техническое обслуживание снижает потерю емкости, вызванную сульфатацией аккумуляторов
Когда емкость батареи снижается, это, вероятно, происходит из-за кристаллов сульфата, которые постепенно накапливаются на электродах. Это не позволяет батарее эффективно отдавать ток, потому что кристаллы «душат» батарею.
Это не позволяет батарее эффективно отдавать ток, потому что кристаллы «душат» батарею.
Сульфат свинца увеличивает внутреннее сопротивление и снижает плотность электролита. Процесс сульфатации неизбежен. Хуже того, через 3-4 года процесс существенно ускоряется (отсюда резкое падение производительности вашей батареи). Если ваша батарея страдает от этого типа сульфатации, наш регенератор батареи будет очень эффективным.
Если вы обслуживаете аккумулятор раз в год с помощью нашего регенератора аккумуляторов, у аккумулятора не будет ни единого шанса!
2) Чистка + разбор + ремонт аккумулятора
Перед десульфатацией батареи очень важно убедиться, что батарея, соединения батареи и батарейный отсек не имеют дефектов.Мы также должны убедиться, что поверхность батареи нейтрализована (AQ Steam), чтобы накопление сульфатации на разъемах не влияло на работу батареи. Необработанная поверхность батареи может вызвать токи утечки, что отрицательно скажется на сроке службы батареи.
Когда все соединения проверены и поверхность обработана, можно приступить к самому процессу регенерации.
3) Восстановление свинцово-кислотных аккумуляторов с помощью Energic Plus
Устройство для восстановления аккумуляторов выполняет 2 цикла зарядки, выравнивания и разрядки.Во время этого процесса сульфат свинца удаляется за счет электрических высокочастотных пульсаций регенератора батареи. Это дает следующие результаты:
— увеличится удельный вес электролита,
— уменьшится внутреннее сопротивление,
— увеличится емкость батареи (Ач) и
— увеличится напряжение элемента
Если регенератор батареи совмещен с нашей системой мониторинга батареи (BMS-система), вы даже можете выполнить полный анализ каждой ячейки батареи.Действительно уникальная функция!
4) Анализ батареи после процесса восстановления батареи
После завершения процесса восстановления батареи проводится повторный анализ ее состояния. Улучшения обрабатываются, и все ячейки проверяются, чтобы увидеть, не нужно ли заменить какие-либо из них. Отчеты о состоянии батареи (в формате pdf, Word или Excel) и отчеты BMS-системы (в формате pdf, Word или Excel) формируются таким образом, чтобы вы точно знали, каково текущее состояние вашей батареи.
Отчеты о состоянии батареи (в формате pdf, Word или Excel) и отчеты BMS-системы (в формате pdf, Word или Excel) формируются таким образом, чтобы вы точно знали, каково текущее состояние вашей батареи.
5) Ввод в эксплуатацию свинцово-кислотного аккумулятора
После завершения процесса десульфатации аккумулятор можно снова использовать! Хватит тратить деньги, начните использовать регенератор аккумуляторов Energic Plus!
Когда следует регенерировать аккумулятор?
Регенерация батареи может быть выполнена в любое время. Обычно это реализуется, когда батарея потеряла 30-40% своей емкости. Тогда обычно удается полностью восстановить его. Хотя в некоторых случаях невозможно достичь полной мощности, эти восстановления часто дают невероятные результаты.Помимо сульфатации, батареи часто повреждаются из-за естественного процесса старения. Потерянные части положительных пластин и сильная коррозия восстановлению не подлежат.
Почему Energic Plus является инновационным по сравнению с другими вариантами?
Оборудование для регенерации аккумуляторов Energic Plus сочетает в себе различные эффективные методы регенерации аккумуляторов с интегрированной рекуперацией энергии в одном устройстве. О технологии: для достижения оптимальных результатов необходимо правильное напряжение, ток, время, частота обновления и температура.Мы делаем это с помощью компьютеризированного процесса: каждая батарея разряжается и восстанавливается индивидуально, в зависимости от ее состояния и размера, в то время как максимальные импульсы напряжения регулируются в различных кривых и циклах. Процесс разряда также различается по импульсообразным минимальным расстояниям. Он защищает аккумуляторы и подготавливает их к регенерации. Эти комбинации и методы уникальны и защищены международными патентами. В зависимости от размера батареи требуются огромные токи и напряжения, которые могут быть обеспечены только трансформаторами соответствующего размера.Особой изюминкой является возврат энергии в процессе разряда. Энергопотребление остается на самом низком уровне.
О технологии: для достижения оптимальных результатов необходимо правильное напряжение, ток, время, частота обновления и температура.Мы делаем это с помощью компьютеризированного процесса: каждая батарея разряжается и восстанавливается индивидуально, в зависимости от ее состояния и размера, в то время как максимальные импульсы напряжения регулируются в различных кривых и циклах. Процесс разряда также различается по импульсообразным минимальным расстояниям. Он защищает аккумуляторы и подготавливает их к регенерации. Эти комбинации и методы уникальны и защищены международными патентами. В зависимости от размера батареи требуются огромные токи и напряжения, которые могут быть обеспечены только трансформаторами соответствующего размера.Особой изюминкой является возврат энергии в процессе разряда. Энергопотребление остается на самом низком уровне.
Могу ли я получить обновление и снижение содержания сульфатов с помощью специальной жидкости?
Да и нет. Добавки кобальта, марганца и других веществ не новы. Он широко использовался во время 2-й мировой войны на батареях подводных лодок. В результате происходит высвобождение поверхностных сульфатных отложений. Уровень кислоты повышается до нормы и емкость несколько увеличивается.Этот эффект возникает в зависимости от степени сульфатации и возраста аккумулятора через небольшой промежуток времени. Кроме того, в электролите остается загрязняющее вещество. Структурные повреждения поверхности не фиксируются и могут даже увеличиться. Кроме того, твердые кристаллы сульфата не растворяются полностью и могут вызвать дальнейшее загрязнение и разрушение аккумулятора. В долгосрочной перспективе соединения серебра и/или кобальта наносят аккумулятору необратимый ущерб.
Он широко использовался во время 2-й мировой войны на батареях подводных лодок. В результате происходит высвобождение поверхностных сульфатных отложений. Уровень кислоты повышается до нормы и емкость несколько увеличивается.Этот эффект возникает в зависимости от степени сульфатации и возраста аккумулятора через небольшой промежуток времени. Кроме того, в электролите остается загрязняющее вещество. Структурные повреждения поверхности не фиксируются и могут даже увеличиться. Кроме того, твердые кристаллы сульфата не растворяются полностью и могут вызвать дальнейшее загрязнение и разрушение аккумулятора. В долгосрочной перспективе соединения серебра и/или кобальта наносят аккумулятору необратимый ущерб.
Есть ли польза от регенерации «молодой» батареи?
Да.Десульфатация аккумуляторов может улучшить качество аккумуляторов, которым от 1 до 2 лет, поскольку сульфатирование происходит с момента изготовления аккумулятора. Аккумуляторы, прошедшие процесс регенерации, сохраняют и обеспечивают постоянную емкость на уровне 90-100% в течение 8-10 лет.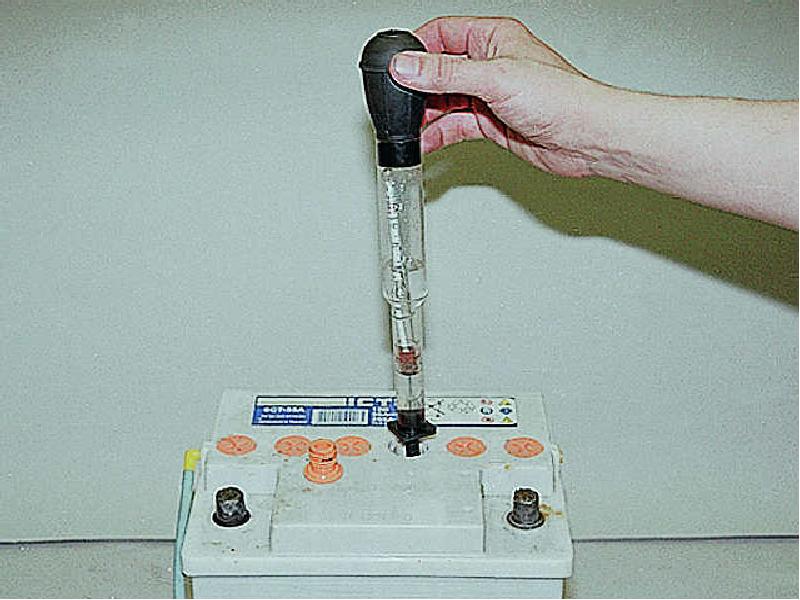
Технологии регенерации аккумуляторов, подходящие для нескольких приложений
Регенерация батареи для вилочных погрузчиков
Регенерация аккумулятора для автомобилей
Регенерация батареи для грузовых автомобилей
Регенерация аккумулятора для гольф-тележек
Регенерация батареи для поездов
Регенерация батареи для автобусов
Регенерация батареи для тракторов
Регенерация аккумулятора для четырехлетних 289
Как начать бизнес по ремонту аккумуляторов
Вы ищете новую возможность? Станьте дилером систем восстановления аккумуляторов Energic Plus и начните бизнес по ремонту аккумуляторов! Заинтересованы? Применить сейчас!
типов аккумуляторов — аккумуляторы для промышленных приложений и приложений электронной мобильности RechargeBatteries
Аккумуляторная технология
Аккумуляторы состоят из собранных элементарных ячеек и бывают разных размеров и форм. Портативные батареи, например, содержат всего несколько ячеек, а большие промышленные батареи могут состоять из сотен ячеек, собранных в модули. Надежное функционирование этих модулей и, следовательно, производительность батареи управляются сложной электронной системой управления, так называемой BMS. BMS отслеживает и контролирует важные данные и процессы, чтобы предотвратить работу батареи за пределами безопасного рабочего режима.
Портативные батареи, например, содержат всего несколько ячеек, а большие промышленные батареи могут состоять из сотен ячеек, собранных в модули. Надежное функционирование этих модулей и, следовательно, производительность батареи управляются сложной электронной системой управления, так называемой BMS. BMS отслеживает и контролирует важные данные и процессы, чтобы предотвратить работу батареи за пределами безопасного рабочего режима.
В зависимости от того, для чего используется аккумулятор, различаются его технические характеристики и, соответственно, состав материала и морфология аккумулятора.Для некоторых аккумуляторов требуется легкий вес, для других — высокая мощность или очень быстрые циклы зарядки. Важные прорывы в аккумуляторных технологиях, особенно в тех, которые используются для электромобилей, и постоянные улучшения привели к появлению огромного количества приложений с батарейным питанием.
Что такое перезаряжаемые батареи?
Все батареи преобразуют химическую энергию в электрическую. Аккумуляторы, также называемые вторичными батареями, могут использоваться до нескольких тысяч циклов зарядки и разрядки.Благодаря своим химическим свойствам перезаряжаемые батареи могут восстанавливать свой первоначальный состав, снова и снова давая энергию многим современным приложениям. Некоторые из этих приложений:
Аккумуляторы, также называемые вторичными батареями, могут использоваться до нескольких тысяч циклов зарядки и разрядки.Благодаря своим химическим свойствам перезаряжаемые батареи могут восстанавливать свой первоначальный состав, снова и снова давая энергию многим современным приложениям. Некоторые из этих приложений:
В свою очередь, первичные или одноразовые батареи нельзя перезаряжать, так как их химические реакции необратимы. Они в основном используются в портативных устройствах с низким потреблением тока, используются только периодически или используются вдали от альтернативного источника питания, например, в цепях сигнализации и связи, где другое электропитание доступно только периодически.Как правило, первичные батареи имеют более высокую плотность энергии, чем перезаряжаемые батареи, но плохо работают в приложениях с высоким энергопотреблением и нагрузкой менее 75 Ом.
Европейская аккумуляторная промышленность
Сегодня на Европу приходится лишь около 5% мировых мощностей по производству элементов и аккумуляторов, но ежегодный спрос на аккумуляторы в ЕС оценивается в размере до 250 миллиардов евро с 2025 года и, как ожидается, создаст около 800 000 прямых и до 3 миллионов косвенных новых рабочие места. Чтобы стимулировать производство аккумуляторных элементов в Европе, в октябре 2017 года Европейский Союз создал Европейский альянс аккумуляторов. Под лозунгом превращения «Европы в мирового лидера в области устойчивого производства и использования аккумуляторов» отраслевые партнеры, RD&I, а также государства-члены ЕС объединили свои усилия для создать устойчивую и конкурентоспособную производственно-сбытовую цепочку производства аккумуляторов в Европе. В 2019 году европейская аккумуляторная экосистема привлекла инвестиции в размере более 60 миллиардов евро.
Чтобы стимулировать производство аккумуляторных элементов в Европе, в октябре 2017 года Европейский Союз создал Европейский альянс аккумуляторов. Под лозунгом превращения «Европы в мирового лидера в области устойчивого производства и использования аккумуляторов» отраслевые партнеры, RD&I, а также государства-члены ЕС объединили свои усилия для создать устойчивую и конкурентоспособную производственно-сбытовую цепочку производства аккумуляторов в Европе. В 2019 году европейская аккумуляторная экосистема привлекла инвестиции в размере более 60 миллиардов евро.
Ведущая отрасль для социального и экономического процветания
Хотя большая часть источников сырья и производства элементов и аккумуляторов по-прежнему осуществляется за пределами Европы, европейским компаниям принадлежит значительная часть интеллектуальной собственности и технологических ноу-хау в аккумуляторной промышленности.Европе также удалось завоевать сильное присутствие в секторе сборки аккумуляторных батарей и переработки отходов, и она предлагает солидные возможности финансирования, а также квалифицированную рабочую силу. В сочетании с высокими экологическими и социальными стандартами это делает Европу идеальным рынком для процветающей аккумуляторной промышленности.
В сочетании с высокими экологическими и социальными стандартами это делает Европу идеальным рынком для процветающей аккумуляторной промышленности.
Знание батареи
Об аккумуляторной батарее
В продаже имеется пять типов перезаряжаемых батарей.В следующей таблице сравниваются их производительность и применение. В настоящее время наиболее популярными аккумуляторами являются никель-кадмиевые, никель-металлогидридные и литий-ионные аккумуляторы в бытовой электронике, которые входят в число наших основных продуктов. Использование перезаряжаемой батареи может сохранить окружающую среду и сэкономить ваши деньги. Например, одну NiMH-батарею размера AA можно использовать не менее 500 раз, и она эквивалентна 500 щелочным батареям типа AA, что будет стоить вам менее 0,002 доллара США за каждый раз. |
Сравнение производительности различных аккумуляторов | |||||
Параметры | Свинцово-кислотный | Ni-Cd | Ni-M-H | Жидкость Литий-ионный | Полимер Литий-ионный |
Напряжение (В) | 2 | 1. | 1,2 | 3,6 | 3,6 |
Весовая плотность энергии (Втч/кг) | 35 | 50 | 80 | 125 | 170 |
Объемная энергия Плотность (Втч/л) | 80 | 150 | 200 | 320 | 400 |
Срок службы (раз) | 300 | 500 | 500 | 800 | 1000 |
Саморазряд | 0 | 25-30 | 30-35 | 6-9 | 2-5 |
Состояние электролита | Жидкость | Жидкость | Жидкость | Жидкость | Полимерный гель |
Мин. | > 10 мм | >3 мм | >3 мм | >3 мм | <1 мм |
Эффект памяти | нет | да | нет | № | № |
Загрязнение | да | да | № | № | № |
Стоимость производства | самый низкий | Низкий | средний | Высокий | Средний |
Преимущества | Высокий ток стока и низкая стоимость | Средний ток стока и низкая стоимость, меньший объем | Средний ток и стоимость стока, большая емкость | большая вместимость и меньший вес | Максимальная вместимость, малый вес и гибкая форма |
Недостатки | Слишком тяжелый | Небезопасно для окружающей среды | Более высокий саморазряд и вес | Низкий ток стока и более высокая стоимость | Низкий ток стока и очень высокая стоимость |
Приложения | Автомобиль и освещение | Электроинструмент, беспроводной телефон, аварийное освещение и т. | Игрушка, КПК, MP3 и цифровая камера и т. д. | Сотовый телефон и портативный компьютер | Портативные компьютеры |
Промышленные стандартные цилиндрические размеры батареи
| Размер ячейки | Диаметр (мм) | Длина (мм) | Длина (мм) | Длина Никада (граммы) | 0 Nimh вес (грамм)
|---|---|---|---|---|
| Размер батареи | ||||
| AAAA | 8.4 | 40,2 | 10 | 10 |
| 4/3 АААА | 8,4 | 67 | 12-13 | 13 |
| 1/4 ААА | 10,5 | 14 | 2,5-3,5 | 2,5-4 |
| 1/3 ААА | 10,5 | 16 | 5,5 | 5,5 |
| 1/2 ААА | 10. 5 5 | 22 | 7 | |
| 2/3 ААА | 10,5 | 30 | 6-8 | 8-9 |
| ААА36 | 10,5 | 36 | 11 | |
| 4/5 ААА | 10,5 | 37 | 11 | |
| ААА38 | 10.5 | 38 | 11 | |
| 3/4 ААА | 10,5 | 39,5 | 12 | 12 |
| ААА42 | 10,5 | 42 | 12 | |
| ААА | 10,5 | 44,5 | 10 | 13 |
| 5/4 ААА | 10.5 | 50 | 14 | 15 |
| Л-ААА | 10,5 | 50 | 13 | 14 |
| 4/3 ААА | 10,5 | 67 | 17 | 18 |
| 5/3 ААА | 10,5 | 67 | 19 | 19 |
| ЛЛ-ААА | 10. 5 5 | 67 | 17 | 18 |
| 3/2 ААА | 10,5 | 67 | 19 | 20 |
| 6/4 ААА | 10,5 | 67 | 20 | 20 |
| 7/5 ААА | 10,5 | 66,5 | 15 | 15 |
| 7/4 ААА | 10.5 | 76 | 19 | 20-21 |
| 7/3 ААА | 10,5 | 80 | 23 | |
| СЛ ААА | 10,5 | 80 | 23 | |
| 1/3 АА | 14,2 | 17,5 | 6,5 | 7 |
| 1/2 АА | 14.2 | 30 | 12 | 15 |
| 2/3 АА | 14,2 | 28,7 | 13-15 | 13-16 |
| 4/5 АА | 14,2 | 43 | 20 | 22 |
| АА | 14,2 | 50 | 21 | 27 |
| AA с плоской вершиной | 14. 2 2 | 48 | 21 | 27 |
5/4 АА | 14,2 | 64,5 | 29 | |
| Л-АА | 14,2 | 65 | 29 | 30 |
| 4/3 АА | 14,2 | 65,2 | 30 | 30 |
| 7/5 АА | 14.2 | 70 | 29 | 39 |
| 1/3 А | 17 | 21 | ||
| 1/2 А | 17 | 25 | 17 | 21 |
| 2/3 А | 17 | 28,5 | 18-20 | 20-23 |
| 4/5 А | 17 | 43 | 26-31 | 32-35 |
| А | 17 | 50 | 32 | 40 |
| 4/3 А | 17 | 67 | 50 | 55 |
| Л-А | 17 | 67 | 48 | 53 |
| 7/5 А | 17 | 70 | 44. 8 8 | 56 |
| Жир А | 18 | 50 | 38 | 42 |
| 4/3 жира A | 18 | 67 | 56 | 60 |
| L-жир А | 18 | 67 | 55 | 60 |
Аккумуляторы размера Sub-C | ||||
| 1/2 SC | 23 | 26 | 30 | |
| 2/3 SC | 23 | 28 | 25 | 28 |
| 4/5 ПК | 23 | 34 | 38 | 42 |
| СК (суб С) | 23 | 43 | 52 | 55 |
| Переходник 5/4 C | 23 | 49.5 | 65-67 | 70 |
| 4/3 ПК | 23 | 50 | 60 | 66 |
| L-SC | 23 | 50 | 57 | 63 |
Батарейки размера C | ||||
| 1/2 С | 26 | 24 | 31 | 34 |
| 3/5 С | 26 | 30 | 40 | 44 |
| 2/3 С | 26 | 31 | 45 | 50 |
| С | 26 | 46 | 72 | 80 |
| 5/4С | 26 | 58 | 90 | 100 |
Батарейки размера D | ||||
| 1/2 D | 33 | 37 | 81-84 | 81 |
| 2/3 D | 33 | 43. 4 4 | 98-105 | 115 |
| Д | 33 | 58 | 105-145 | 105-160 |
| 4/3 D | 33 | 89 | 140-190 | 175 |
| 3/2 D | 33 | 90,3 | 195-236 | 240 |
Батареи размера F | ||||
| Ф | 33 | 91.2 | 231 | 255 |
| SF (супер F) | 41,4 | 89,1 | 393 | 425 |
| ||||
Каков срок службы перезаряжаемой батареи?
Когда аккумулятор заряжается и разряжается, мы называем цикл или период. В заявленных принципах заряда и разряда и снижении емкости до установленного стандарта общее количество циклов, которое он может пройти, называется сроком службы перезаряжаемой батареи.
В заявленных принципах заряда и разряда и снижении емкости до установленного стандарта общее количество циклов, которое он может пройти, называется сроком службы перезаряжаемой батареи.
Что такое саморазряд аккумуляторной батареи?
Первичная батарея или полностью заряженная вторичная батарея, если ее отложить на некоторое время, ее емкость уменьшится или потеряется, это явление вызывает саморазряд, то есть электричество уходит. Это решает внутренняя электрохимическая система, аналогичная утечке воды из пруда или резервуара.
Что такое внутреннее сопротивление батареи?
Полное сопротивление батареи — это сопротивление при протекании тока через работающую ячейку, как правило, внутреннее сопротивление включает как постоянное, так и постоянное сопротивление. и переменный ток сопротивление. Поскольку сопротивление перезаряжаемой ячейки невелико, а электрод легко поляризуется, создавая сопротивление поляризации при измерении постоянного тока. сопротивление, точное значение не может быть измерено.
сопротивление, точное значение не может быть измерено.
Что такое эффект памяти?
Эффект памяти возникает только на никель-кадмиевых аккумуляторах.Так как в традиционной технологии отрицательным моментом Ni-Cd аккумуляторов является агломерация с толстым кристаллом Ni, если Ni-Cd аккумуляторы перезаряжаются до того, как они полностью разрядятся, кристаллы Ni легко собираются в агломераты, что создает первичную разрядную платформу. Аккумулятор сохраняет платформу, которая будет считаться окончанием разрядки для следующего цикла, даже если емкость решает, что аккумулятор может быть разряжен до более низкой платформы. Аккумулятор сохранит этот процесс в своей памяти, поэтому при следующем разряде аккумулятор запомнит только эту уменьшенную емкость.Точно так же любая дальнейшая неполная разрядка при каждом использовании усугубит эффект и снизит емкость. Эффект Существует два метода устранения эффекта: во-первых, глубокий разряд при маленьком токе (т. е. от 0,1С до 0В), во-вторых, несколько циклов при больших токах (например, 1С).
е. от 0,1С до 0В), во-вторых, несколько циклов при больших токах (например, 1С).
Как температура окружающей среды влияет на работу батареи?
Низкие температуры (например, -15?), очевидно, уменьшат скорость разряда Ni-Cd и Ni-MH аккумуляторов. В -20? электролит находится в точке замерзания, скорость заряда сильно замедлится.При низкой температуре (ниже -15?) заряд повысит внутреннее давление газа и, возможно, откроет предохранительный клапан. Температура окружающей среды от 5? до 30? это лучший диапазон для получения эффективного заряда. Как правило, с повышением температуры эффективность заряда становится выше. А когда температура поднимется до 45? или выше, производительность материалов в аккумуляторе ухудшится, и срок службы аккумулятора значительно сократится.
Как «Перезарядка» влияет на работу аккумулятора?
«Перезарядка» — это непрерывная зарядка после того, как батарея полностью заряжена определенным методом зарядки. Поскольку уровень емкости от положительной полярности выше, чем от отрицательной полярности, положительная полярность будет генерировать кислород, который может быть составлен с кадмием, полученным от отрицательной полярности через сепаратор. В общем случае внутреннее давление не увеличится значительно, однако, если зарядный ток, подаваемый на батарею, слишком велик, время зарядки очень велико и, наконец, кислород не может быть израсходован вовремя, батарея выйдет из строя. из-за повышения давления, искажения батареи, утечки и так далее.Однозначно производительность батареи тоже снизится
Поскольку уровень емкости от положительной полярности выше, чем от отрицательной полярности, положительная полярность будет генерировать кислород, который может быть составлен с кадмием, полученным от отрицательной полярности через сепаратор. В общем случае внутреннее давление не увеличится значительно, однако, если зарядный ток, подаваемый на батарею, слишком велик, время зарядки очень велико и, наконец, кислород не может быть израсходован вовремя, батарея выйдет из строя. из-за повышения давления, искажения батареи, утечки и так далее.Однозначно производительность батареи тоже снизится
Как влияет «Переразряд» на работу аккумулятора?
Если напряжение элемента достигает расчетного значения, это означает, что батарея разрядила накопленную емкость, но процесс разряда продолжается постоянно, что может привести к переразряду. Обычно конечное напряжение можно определить по току разряда, например, конечное напряжение устанавливается на уровне 1,0 В на элемент при разряде при 0,2–2 °С и 0.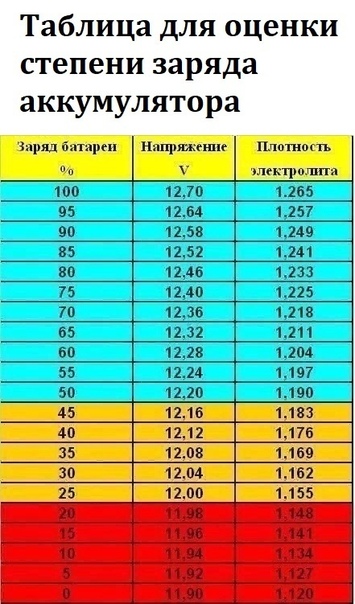 8В/ячейка при 3C или выше, т.е. 5С или 10С. Переразряд может привести к катастрофе, особенно при сильном токе или многократном переразряде. Обычно чрезмерная разрядка может привести к повышению внутреннего давления в клетке, и обратимость активности материалов как в положительную, так и в отрицательную сторону будет нарушена. Даже при зарядке может восстановиться только часть, и емкость явно снижается.
8В/ячейка при 3C или выше, т.е. 5С или 10С. Переразряд может привести к катастрофе, особенно при сильном токе или многократном переразряде. Обычно чрезмерная разрядка может привести к повышению внутреннего давления в клетке, и обратимость активности материалов как в положительную, так и в отрицательную сторону будет нарушена. Даже при зарядке может восстановиться только часть, и емкость явно снижается.
Как короткое замыкание влияет на работу аккумулятора?
Любые проводящие материалы, соединенные с внешними клеммами батареи, приведут к короткому замыканию.В зависимости от аккумуляторной системы короткое замыкание может иметь серьезные последствия, например. повышение температуры электролита или повышение внутреннего давления газа. Если значение внутреннего давления газа превышает предел прочности крышки элемента, произойдет утечка электролита, что приведет к значительному повреждению аккумулятора. Если безопасная вентиляция не сработает, произойдет даже взрыв. Поэтому не замыкайтесь.
Поэтому не замыкайтесь.
Какова производительность никель-кадмиевой батареи?
- Низкая стоимость;
- Отличная устойчивость к перезарядке;
- Отличные характеристики быстрой зарядки;
- Длительный срок службы;
- Широкий диапазон температур;
- Саморазряд средней степени;
- Хорошие показатели безопасности.
Какова производительность никель-металлогидридной батареи?
- Низкая стоимость;
- Хорошая производительность при быстрой зарядке;
- Длительный срок службы;
- Нет накопления памяти;
- Зеленые источники энергии, не загрязняющие окружающую среду;
- Широкий диапазон температур;
- Хорошие показатели безопасности.
Какова производительность литий-ионного аккумулятора?
- Высокая плотность энергии;
- Высокое рабочее напряжение;
- Нет накопления памяти;
- Длительный срок службы;
- Нет загрязнения;
- Легкий вес;
- Очень низкий уровень саморазряда.

Какова производительность полимерной литий-ионной батареи?
- Не содержит жидкого электролита, поэтому утечка исключена;
- Можно придать различную форму;
- Можно превратить в тонкую батарею, например, 3,6 В, 400 мАч, толщина может уменьшиться до 0,5 мм;
- Высокое напряжение в аккумуляторе: несколько аккумуляторов с жидким электролитом можно соединить последовательно, чтобы получить только высокое напряжение; литий-полимерный аккумулятор может получить высокое напряжение в ячейке через многопользовательскую комбинацию;
- Емкость литий-полимерных аккумуляторов одинакового объема в два раза превышает емкость литий-ионных аккумуляторов.
Какова производительность литиевой батареи MnO2 и Li-SOCL2?
- Высокая плотность энергии;
- Длительный срок хранения;
- Широкий диапазон рабочих температур;
- Хорошее уплотнение;
- Стабильное напряжение разряда
Почему батарейные блоки имеют нулевое или низкое напряжение?
(1) Напряжение одной из ячеек равно 0 В;
(2) Короткое замыкание или обрыв цепи вилки, или плохое прикосновение;
(3) Токопроводящие провода оборваны от пайки или слабо припаяны;
(4) Неправильное подключение аккумулятора или соединительные выступы отсутствуют, слабо приварены или сломаны.
Меры предосторожности:
1. Внимательно прочитайте спецификацию или проконсультируйтесь по правильному использованию.
2. В соответствии с указаниями электроприбора, правильно вставьте положительный и отрицательный полюсы аккумулятора.
3. Не используйте вместе новую и старую батарею или батарею другого типа и модели.
4. Не заряжайте основной аккумулятор.
5. Не нагревайте и не разбирайте аккумулятор, даже не бросайте его в огонь или воду.
6.Не допускайте короткого замыкания в случае взрыва батареи, протечки или других повреждений.
7. При обнаружении исключительных условий, таких как ужасный запах, утечка, трещины и деформация корки батареи, немедленно прекратите использование батареи.
8. Поместите аккумулятор в недоступном для детей месте.
9. Если вытекшая жидкость попала в глаза, тщательно промывайте глаза чистой водой в течение не менее 15 минут, поднимая верхние и нижние веки до тех пор, пока не исчезнут следы химического вещества. Обратитесь за медицинской помощью.
Обратитесь за медицинской помощью.
10.Если электроприбор не используется в течение длительного времени, извлеките аккумулятор и храните его в прохладном, хорошо проветриваемом месте.
Почему литий-ионный аккумулятор имеет нулевое напряжение?
Из соображений безопасности наш литий-ионный аккумулятор имеет защиту печатной платы, которая защищает аккумуляторы от перезарядки и разрядки. Когда литий-ионный аккумулятор перезаряжается или разряжается, печатная плата автоматически отключается. Затем вы можете обнаружить, что аккумуляторная батарея имеет 0 напряжения.Это не означает, что батарея разряжена. Вы можете просто использовать наше зарядное устройство, чтобы зарядить его, и все вернется на круги своя. Убедитесь, что вы используете зарядные устройства, рекомендованные компанией batteryspace. Мы не несем ответственности за зарядные устройства других марок. Однако это не относится к аккумулятору, который не заряжался более двух месяцев. Вы должны заряжать аккумулятор каждые 2 месяца, чтобы он оставался свежим, если вы им не пользуетесь.
Вы должны заряжать аккумулятор каждые 2 месяца, чтобы он оставался свежим, если вы им не пользуетесь.
Как восстановить аккумуляторную батарею низкого напряжения 7,2–9,6 В NMh (0,5 В/уровень ячейки) методом электрошока?
Если напряжение NiMH аккумулятора меньше 1.0 В/ячейка. Это не означает, что аккумулятор неисправен или зарядное устройство не смогло распознать аккумулятор. Поразите аккумулятор или аккумулятор электрическим током с помощью адаптера переменного тока 12 В постоянного тока 0,5 А в течение 1 минуты. Тогда ваше зарядное устройство распознает ячейку или аккумулятор и сможет заряжать номинальным зарядным током. Дополнительная информация. Пожалуйста, загрузите руководство по восстановлению NiMH-батареи/NiMH-аккумулятора.
Как ухаживать за аккумуляторной батареей Powerizer Nimh/Nicd:
Все никель-кадмиевые/никель-металлогидридные аккумуляторы (упаковки), которые мы отправляем, полностью заряжены , а не . Это связано с соображениями безопасности во время транспортировки. Чтобы батарея (комплект) прослужила вам долгое время, вам необходимо выполнить следующие шаги при получении нашей батареи (комплекта).
Это связано с соображениями безопасности во время транспортировки. Чтобы батарея (комплект) прослужила вам долгое время, вам необходимо выполнить следующие шаги при получении нашей батареи (комплекта).
Для NiCd или NiMh аккумуляторов (упаковка):
- Полностью зарядите аккумулятор (блок) перед использованием.
- Полностью разрядите аккумулятор (блок) (до 1,0 В на элемент) перед повторной зарядкой или до тех пор, пока устройство не перестанет работать.
- Повторите шаги 1 и 2 четыре (4) раза, чтобы привести аккумулятор в рабочее состояние, чтобы он мог достичь полной емкости
- Мы рекомендуем перезаряжать аккумулятор (комплект) не реже одного раза в 2 месяца для поддержания емкости аккумулятора.
Как ухаживать за литиевой аккумуляторной батареей Powerizer?
Пожалуйста, загрузите литий-ионный аккумулятор Take Care.pdf
Какой аккумулятор лучше?
Ниже приводится сводная информация о достоинствах и недостатках современных популярных аккумуляторных систем.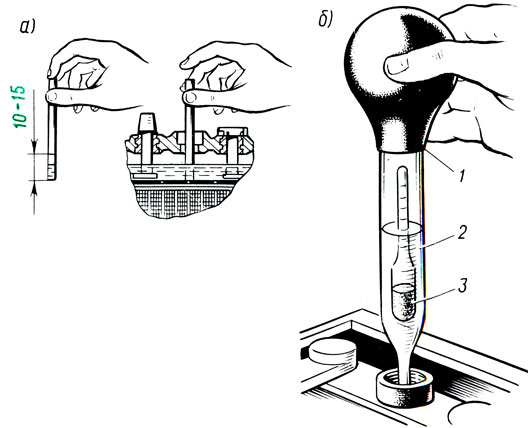 Хотя плотность энергии имеет первостепенное значение, другими важными атрибутами являются срок службы, характеристики нагрузки, требования к техническому обслуживанию, затраты на саморазряд и безопасность.Никель-кадмиевая батарея — первая перезаряжаемая батарея малого формата, являющаяся эталоном, с которым обычно сравнивают другие химические элементы. Тенденция к системам на основе лития.
Хотя плотность энергии имеет первостепенное значение, другими важными атрибутами являются срок службы, характеристики нагрузки, требования к техническому обслуживанию, затраты на саморазряд и безопасность.Никель-кадмиевая батарея — первая перезаряжаемая батарея малого формата, являющаяся эталоном, с которым обычно сравнивают другие химические элементы. Тенденция к системам на основе лития.
Никель-кадмий — зрелый, но имеет умеренную плотность энергии. Никель-кадмиевые аккумуляторы используются там, где важны длительный срок службы, высокая скорость разряда и расширенный температурный диапазон. Основными областями применения являются двусторонние радиостанции, биомедицинское оборудование и электроинструменты. Никель-кадмий содержит токсичные металлы.
Никель-металлогидридный — имеет более высокую удельную энергию по сравнению с никель-кадмиевыми за счет уменьшенного срока службы.Нет токсичных металлов. Приложения включают мобильные телефоны и портативные компьютеры. NiMH рассматривается как ступенька к системам на основе лития.
NiMH рассматривается как ступенька к системам на основе лития.
Свинцово-кислотные — наиболее экономичны для приложений с большой мощностью, где вес не имеет большого значения. Свинцово-кислотные являются предпочтительным выбором для больничного оборудования, инвалидных колясок, аварийного освещения и систем бесперебойного питания. Свинцово-кислотные недорогие и прочные. Он занимает уникальную нишу, которую трудно заменить другими системами.
Литий-ионный — самая быстрорастущая аккумуляторная система; предлагает высокую плотность энергии и малый вес.Схема защиты необходима для ограничения напряжения и тока по соображениям безопасности. Приложения включают ноутбуки и мобильные телефоны. Доступны версии с высоким током для электроинструментов и медицинских устройств.
В таблице 1 приведены характеристики обычных аккумуляторов. Цифры основаны на средних рейтингах на момент публикации. Литий-ионный делится на три версии: традиционный кобальт, который обычно используется в сотовых телефонах, камерах и ноутбуках; марганец (шпинель), который приводит в действие высококачественные электроинструменты, и новый фосфат, который конкурирует со шпинелью. Литий-ионный полимер не указан как отдельная система. Его уникальная конструкция работает так же, как литий-ионный на основе кобальта.
Литий-ионный полимер не указан как отдельная система. Его уникальная конструкция работает так же, как литий-ионный на основе кобальта.
Таблица 1: Характеристики часто используемых аккумуляторов.
1) Внутреннее сопротивление аккумуляторной батареи зависит от емкости в мА·ч, проводки и количества элементов. Схема защиты литий-ионная добавляет порядка 100мВт.
2) Основано на размере ячейки 18650. Размер и конструкция ячейки определяют внутреннее сопротивление.Элементы большего размера могут иметь импеданс <15 мОм,
. 3) Срок службы основан на регулярном обслуживании батареи. Несоблюдение периодических циклов полной разрядки может сократить срок службы в три раза.
4) Срок службы зависит от глубины разряда. Неглубокие разряды обеспечивают больше циклов, чем глубокие разряды.
5) Максимальный саморазряд сразу после зарядки, а затем снижается. Потеря емкости никель-кадмия составляет 10% в первые 24 часа, затем снижается примерно до 10% каждые 30 дней. Высокая температура увеличивает саморазряд.
Высокая температура увеличивает саморазряд.
6) Внутренние схемы защиты обычно потребляют 3% накопленной энергии в месяц.
7) Традиционное номинальное напряжение 1,25В; 1,2 В чаще используется для согласования с литий-ионными (3 последовательно = 3,6 В).
8) Литий-ионные часто имеют номинал выше 3,6В. Основано на среднем напряжении под нагрузкой.
9) Выдерживает импульсы сильного тока; нужно время для восстановления.
10) Применяется только для сброса; диапазон температур заряда более ограничен.Обеспечивает более низкую производительность при более низких температурах.
11) Техническое обслуживание может осуществляться в виде «выравнивающей» или «доливочной» загрузки для предотвращения сульфатации.
Источник: Исидор Бухманн, генеральный директор Cadex Electronics Inc., Ванкувер, Британская Колумбия.
Как заменить новый указатель уровня топлива для литий-ионного аккумулятора?
Нажмите здесь, чтобы загрузить инструкцию
Границы | Батареи на основе натрия: в поисках наилучшего компромисса между устойчивостью и максимальным увеличением электрических характеристик
Введение
Среди вторичных батарей литий-ионные батареи (ЛИА) играют важную роль во многих областях систем накопления энергии. С момента их первой коммерциализации Sony в 1991 году дальнейшие исследования были посвящены технологии LIB. Однако максимально достижимая плотность энергии для ЛИА в ближайшем будущем (около 250–260 Втч·кг·−1) недостаточна (Ding et al., 2019), что ограничивает диапазон практических электромобилей (EV). На самом деле существует высокий спрос и интерес к другим технологиям хранения энергии с более высокой плотностью энергии. Системы литий-воздух (Li-O 2 ) и литий-сера (Li-S) имеют более высокую теоретическую удельную плотность энергии (3600 и 2600 Втч·кг -1, соответственно) по сравнению с ЛИА (Liu et al., 2018). Тем не менее, чтобы иметь зрелую технологию, необходимо преодолеть проблемы, связанные с продолжительностью цикла и безопасностью. Более того, одна из основных проблем заключается в том, что рынки столкнутся с истощением источников лития и, как следствие, высокой себестоимостью производства, если технология переработки не будет внедрена в больших масштабах (Al-Thyabat et al.
С момента их первой коммерциализации Sony в 1991 году дальнейшие исследования были посвящены технологии LIB. Однако максимально достижимая плотность энергии для ЛИА в ближайшем будущем (около 250–260 Втч·кг·−1) недостаточна (Ding et al., 2019), что ограничивает диапазон практических электромобилей (EV). На самом деле существует высокий спрос и интерес к другим технологиям хранения энергии с более высокой плотностью энергии. Системы литий-воздух (Li-O 2 ) и литий-сера (Li-S) имеют более высокую теоретическую удельную плотность энергии (3600 и 2600 Втч·кг -1, соответственно) по сравнению с ЛИА (Liu et al., 2018). Тем не менее, чтобы иметь зрелую технологию, необходимо преодолеть проблемы, связанные с продолжительностью цикла и безопасностью. Более того, одна из основных проблем заключается в том, что рынки столкнутся с истощением источников лития и, как следствие, высокой себестоимостью производства, если технология переработки не будет внедрена в больших масштабах (Al-Thyabat et al. , 2013; Ahmadi et al. ., 2017; Dolega, 2019; Ambrose and Kendall, 2020a; Ambrose and Kendall, 2020b).
, 2013; Ahmadi et al. ., 2017; Dolega, 2019; Ambrose and Kendall, 2020a; Ambrose and Kendall, 2020b).
Принимая во внимание, что существующие LIB уже трудно масштабировать для приложений другого типа (например,г., хранение в масштабе сети) в основном из-за затрат на производство и техническое обслуживание (Etacheri et al., 2011; Habib and Sou, 2018; Chen et al., 2020; Cole and Frazier, 2019), передовых инноваций в области аккумуляторов. Системы накопления энергии (BESS) незаменимы для создания высокоэффективных, экономичных и экологически безопасных аккумуляторов. Для преодоления нынешних ограничений обычных ЛИА были разработаны новые химические вещества, выходящие за рамки литий-ионных (например, натрий, калий, магний и цинк) (Ellis and Nazar, 2012; Yabuuchi et al., 2014; Баркер, 2017; Хван и др., 2017 г.; Дельмас, 2018; Ты и Мантирам, 2018 г .; Ли и др., 2019; Маклафлин, 2019; Мин и др., 2019). Среди многих кандидатов в аноды аноды на основе натрия (Na) привлекли огромное внимание, в основном, благодаря высокому содержанию Na (четвертый распространенный металлический элемент), низкой стоимости поставки (Na 2 CO 3 , 150 долларов США за тонну -1 ; Li 2 CO 3 , 5000 долл. США за тонну −1 ), а также его безопасность (Zhao et al., 2017). Однако технология LIB является зрелой технологией, и в настоящее время нет эквивалентных альтернатив LIB.Поскольку литий очень легкий и имеет высокую теоретическую удельную емкость (3860 мА·ч·г −1 ) (Liu et al., 2018), его очень сложно компенсировать высокой емкостью и недорогим производством аккумуляторов. Действительно, исследования показывают, что общая стоимость натрий-ионных аккумуляторов (SIB) по-прежнему выше, чем у LIB (в пересчете на 9 803 -1 кВтч), даже несмотря на то, что сам Na является более дешевым анодным материалом.
США за тонну −1 ), а также его безопасность (Zhao et al., 2017). Однако технология LIB является зрелой технологией, и в настоящее время нет эквивалентных альтернатив LIB.Поскольку литий очень легкий и имеет высокую теоретическую удельную емкость (3860 мА·ч·г −1 ) (Liu et al., 2018), его очень сложно компенсировать высокой емкостью и недорогим производством аккумуляторов. Действительно, исследования показывают, что общая стоимость натрий-ионных аккумуляторов (SIB) по-прежнему выше, чем у LIB (в пересчете на 9 803 -1 кВтч), даже несмотря на то, что сам Na является более дешевым анодным материалом.
Ключевой вопрос: какова экономическая эффективность переработки лития в будущем? Перспектива производства больших модулей увеличит стоимость ЛИА из-за неуверенности в поставках лития.В настоящее время треть производимого в мире лития уже используется в производстве ЛИА. И последнее, но не менее важное: наличие других основных сырьевых материалов для LIB, особенно кобальта, сталкивается с нестабильностью рынка из-за политических и экологических требований. Если удастся замкнуть цикл для ЛИА и наладить экономику замкнутого цикла, в этом случае производители не будут искать альтернатив. В случае с натрием не будет необходимости в «недорогой переработке», поскольку Na можно легко получить путем выпаривания морской воды (11 000 мг л 9 1803 −1 91 804 в морской воде), где содержание лития в морской воде намного ниже, чем содержание лития в морской воде. На (0.18 мг L -1 ) (Adelhelm et al., 2015). С этой точки зрения батареи на основе натрия хорошо подходят для массового производства и изготовления больших модулей.
Если удастся замкнуть цикл для ЛИА и наладить экономику замкнутого цикла, в этом случае производители не будут искать альтернатив. В случае с натрием не будет необходимости в «недорогой переработке», поскольку Na можно легко получить путем выпаривания морской воды (11 000 мг л 9 1803 −1 91 804 в морской воде), где содержание лития в морской воде намного ниже, чем содержание лития в морской воде. На (0.18 мг L -1 ) (Adelhelm et al., 2015). С этой точки зрения батареи на основе натрия хорошо подходят для массового производства и изготовления больших модулей.
Высокотемпературный натрий/сера уже десятилетиями используется в промышленности с жидким натрием при температуре 300°C (Oshima et al., 2004). Его удельная емкость действительно ниже, чем у реальных ЛИА, так как эта аккумуляторная система требует прочного корпуса и теплоизоляции. Более того, наличие жидкого Na препятствует его применению в электромобилях.Такой тип аккумуляторов можно считать наиболее вероятным для недорогих стационарных систем накопления энергии.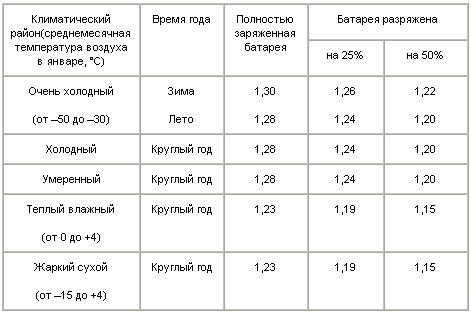
Также сообщалось о концепции перезаряжаемых натрий-воздушных (Na-O 2 ) систем (Zhao et al., 2014; Landa-Medrano et al., 2016). Ячейка Na-O 2 действительно демонстрирует некоторые многообещающие преимущества по сравнению с Li/O 2 , поскольку продукт реакции разряда NaO 2 обладает более высокой энергоэффективностью и обратимостью (Zhao et al., 2014). Тем не менее, он все еще находится на начальной стадии разработки и сталкивается со значительными проблемами, такими как увеличение количества циклов, минимизация побочных продуктов реакции.Как и в Na-S, этот тип батареи также вряд ли будет использоваться в электромобилях.
Помимо технологий Na-S и Na-O 2 , SIB можно рассматривать как более реалистичную технологию хранения энергии, альтернативную современным LIB (Ellis and Nazar, 2012; Ponrouch et al., 2015; Hwang et al., 2017). ; Бин и др., 2018). Наиболее распространенными катодами для СИБ являются оксиды натрия (NaMO 2 , M = V, Fe, Mn, Cu, Co. , Ni), фосфаты натрия (Na 7 V 3 (P 2 O 7 ) 4 , NaFePO 4 , оксиды переходных металлов (V 2 O 5 ) и берлинская лазурь (PB, Na 2 M[Fe(CN) 6 ) , 2012; Дельмас, 2018).Британская компания Faradion недавно объявила, что ее высокоэнергетические элементы Na-MO 2 будут использоваться в коммерческих электромобилях в Индии, и заявила, что они оценивают снижение затрат на уровне элемента на 30% (Barker, 2017). Ранее компания провела несколько демонстраций прототипов, в том числе электровелосипедов и тележек для гольфа, но проект в Австралии представляет собой более серьезную инженерную задачу для современной технологии SIB. Помимо Faradion, начинающая компания Tiamat (Франция) и HiNa Battery Technology (Китай) и другие ключевые новаторы создали прототипы SIB для низкоскоростных электромобилей, аккумуляторов Start&Stop 12 В, электровелосипедов и электросамокатов.
, Ni), фосфаты натрия (Na 7 V 3 (P 2 O 7 ) 4 , NaFePO 4 , оксиды переходных металлов (V 2 O 5 ) и берлинская лазурь (PB, Na 2 M[Fe(CN) 6 ) , 2012; Дельмас, 2018).Британская компания Faradion недавно объявила, что ее высокоэнергетические элементы Na-MO 2 будут использоваться в коммерческих электромобилях в Индии, и заявила, что они оценивают снижение затрат на уровне элемента на 30% (Barker, 2017). Ранее компания провела несколько демонстраций прототипов, в том числе электровелосипедов и тележек для гольфа, но проект в Австралии представляет собой более серьезную инженерную задачу для современной технологии SIB. Помимо Faradion, начинающая компания Tiamat (Франция) и HiNa Battery Technology (Китай) и другие ключевые новаторы создали прототипы SIB для низкоскоростных электромобилей, аккумуляторов Start&Stop 12 В, электровелосипедов и электросамокатов.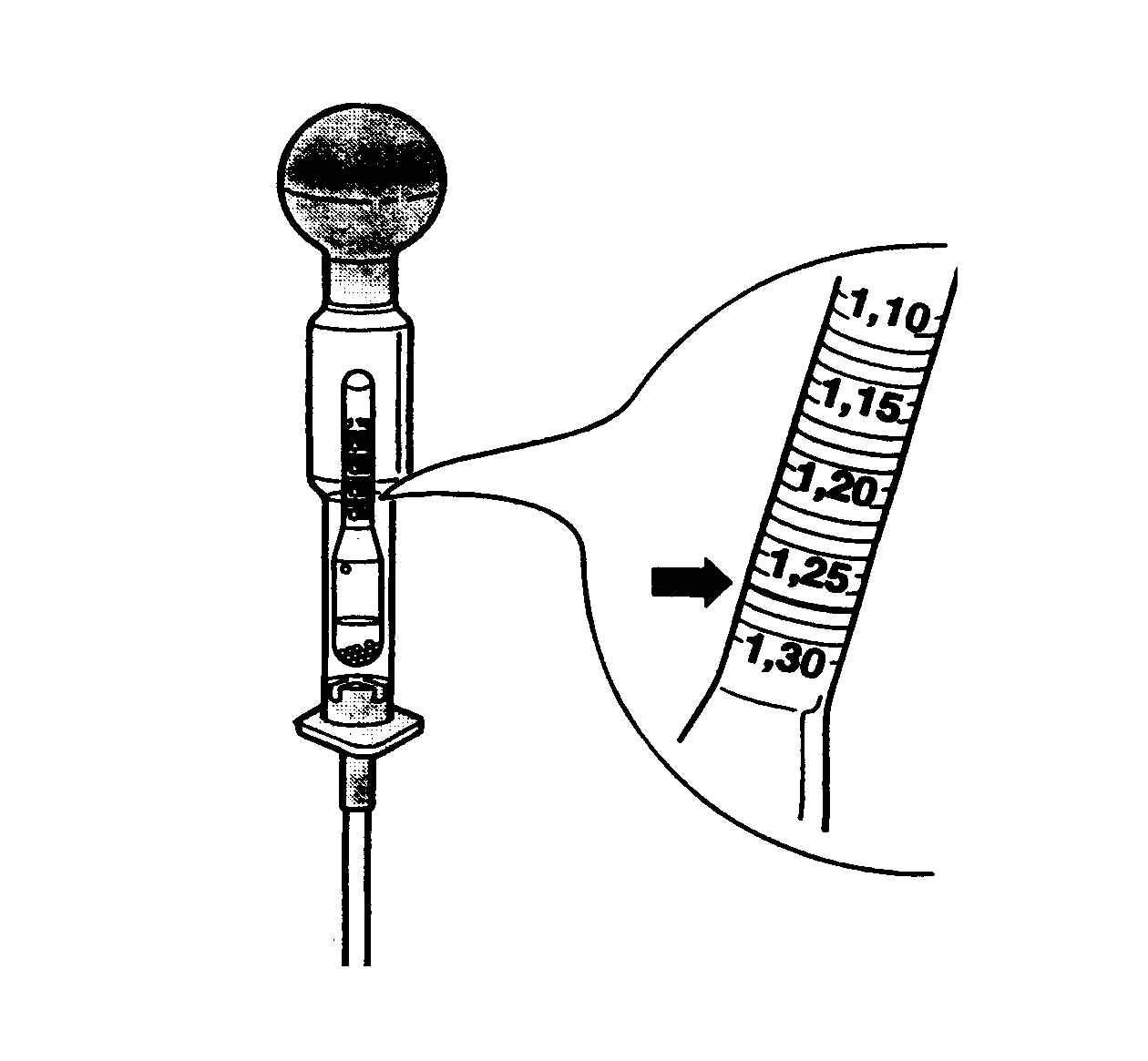
Для СИБ можно использовать два различных типа электролитов: i) водный и ii) органический (Ellis and Nazar, 2012; Delmas, 2018). Водная среда может быть благоприятной благодаря:
• Низкий риск взрыва или воспламенения батареи при нагреве;
• Отсутствие жесткого контроля влажности при сборке, что снижает стоимость аккумулятора;
• Высокая ионная проводимость
Тем не менее, узкое потенциальное окно остается основным препятствием, и очень немногие материалы могут работать в водной среде (Vignarooban et al., 2016; Бин и др., 2018).
В настоящее время большинство натрий-ионных аккумуляторов содержат органический электролит. Эти электролиты обычно состоят из соли натрия, растворенной в одном или нескольких органических растворителях. Наиболее часто используемыми органическими растворителями являются карбонаты, такие как про; пиленкарбонат (PC), этиленкарбонат (EC), диметилкарбонат (DMC), фторэтиленкарбонат (FEC) или виниленкарбонат (VC) (Ponrouch et al. , 2015; Vignarooban et al., 2016; Zhao et al. , 2017).
, 2015; Vignarooban et al., 2016; Zhao et al. , 2017).
В этом документе обсуждаются не только литий-ионные химические вещества, но и основное внимание уделяется SIB на основе органических электролитов.Эта технология анализируется с точки зрения производительности и стоимости, а затем сравнивается с современной технологией LIB, чтобы сделать прогноз, в каких сценариях использования SIB потенциально превзойдут существующие LIB.
Методология основана на литературных исследованиях с последующим анализом материала/стоимости и влияния натриевых батарей на экономику замкнутого цикла. Это исследование представлено авторами с междисциплинарным опытом (материаловедение, электрохимия, очистка сырья и переработка).
Натрий-ионные аккумуляторы с органическим электролитом
Новейшие разработки
Разработка возобновляемых и экологически безопасных SIB на основе органических электролитов привлекла значительно повышенное внимание за последние 6 лет (Adelhelm et al. , 2015; Barker, 2017; Бауэр и др., 2018). Чтобы прийти к выводу о производительности и стоимости SIB и ответить на критические вопросы из введения, на первом этапе этого исследования проводится обзор существующей литературы о SIB на основе органических электролитов.Электролиты этого типа готовятся путем растворения одной из ионных солей натрия (NaClO 4 , NaPF 6 и NaTFSI) в неводных растворителях, таких как EC, PC, DMC, DEC, DME, как в литий-ионных батареях. (Виньярообан и др., 2016). Сообщалось, что ионная проводимость электролита, приготовленного с 1 М NaClO 4 в ЭХ:ДМЭ (50:50 мас.%), достигала 12,5 мс см -1 , что почти такое же значение, как у электролита, приготовленного с 1 М LiPF 6 в EC:DMC (50:50 мас.%) (Vignarooban et al., 2016).
, 2015; Barker, 2017; Бауэр и др., 2018). Чтобы прийти к выводу о производительности и стоимости SIB и ответить на критические вопросы из введения, на первом этапе этого исследования проводится обзор существующей литературы о SIB на основе органических электролитов.Электролиты этого типа готовятся путем растворения одной из ионных солей натрия (NaClO 4 , NaPF 6 и NaTFSI) в неводных растворителях, таких как EC, PC, DMC, DEC, DME, как в литий-ионных батареях. (Виньярообан и др., 2016). Сообщалось, что ионная проводимость электролита, приготовленного с 1 М NaClO 4 в ЭХ:ДМЭ (50:50 мас.%), достигала 12,5 мс см -1 , что почти такое же значение, как у электролита, приготовленного с 1 М LiPF 6 в EC:DMC (50:50 мас.%) (Vignarooban et al., 2016).
Большой атомный радиус Na (0,97 Å для Na + и 0,68 Å для Li + ) вызывает вялую кинетику диффузии натрия и большое объемное расширение, которые являются критическими параметрами для революционных характеристик удельной мощности, которые могут соответствовать реальные потребности электрических сетей и крупных ЭЭС (Chen et al. , 2019). Поэтому важно исследовать новые катодные материалы для SIB с улучшенной кинетикой Na (Chen et al., 2020). Плотность энергии натрий-ионных аккумуляторов напрямую связана с характеристиками материала катода.Как и ЛИА, натриевые катоды делятся на три основные группы: слоистые, оливиновые (NASICON) и шпинельные. Среди них слоистые оксиды (Guo et al., 2014; Liu et al., 2015; Ortiz-Vitoriano et al., 2017; Konarov et al., 2018; Deng et al., 2018; Li et al., 2019) и структурные фосфаты NASICON показали многообещающие результаты (Chen et al., 2019). Совсем недавно аналоги берлинской лазури [PBAs, Na2M[Fe(CN)6], M = Fe, Co, Mn, Ni, Cu и т. д.] были тщательно изучены из-за их больших зазоров в пространственной структуре решетки, которые могут обеспечить многочисленные сайты и транспортные каналы для обратимой деинтеркаляции ионов натрия (Luo et al., 2017; Ван и др., 2018 г.; Ю и др., 2014).
, 2019). Поэтому важно исследовать новые катодные материалы для SIB с улучшенной кинетикой Na (Chen et al., 2020). Плотность энергии натрий-ионных аккумуляторов напрямую связана с характеристиками материала катода.Как и ЛИА, натриевые катоды делятся на три основные группы: слоистые, оливиновые (NASICON) и шпинельные. Среди них слоистые оксиды (Guo et al., 2014; Liu et al., 2015; Ortiz-Vitoriano et al., 2017; Konarov et al., 2018; Deng et al., 2018; Li et al., 2019) и структурные фосфаты NASICON показали многообещающие результаты (Chen et al., 2019). Совсем недавно аналоги берлинской лазури [PBAs, Na2M[Fe(CN)6], M = Fe, Co, Mn, Ni, Cu и т. д.] были тщательно изучены из-за их больших зазоров в пространственной структуре решетки, которые могут обеспечить многочисленные сайты и транспортные каналы для обратимой деинтеркаляции ионов натрия (Luo et al., 2017; Ван и др., 2018 г.; Ю и др., 2014).
Слоистые оксидные соединения, представляющие интерес в качестве катодных материалов для СИП, имеют общую формулу Na x MO 2 , где М обозначает один или несколько переходных металлов (Ti, V, Cr, Mn, Fe, Co или Ni ). Оксиды переходных металлов со слоистой двумерной структурой широко изучаются из-за их улучшенных электрохимических характеристик по сравнению с другими соединениями. Эти материалы классифицируются как структуры типа O3 и P2, где буквы O и P обозначают расположение иона натрия в кристаллической структуре (P-призматическая позиция, O-октаэдрическая позиция) (рис. 1).Цифры обозначают слой переходного металла в повторяющейся элементарной ячейке структуры (Delmas, 2018). Типы O3 и P2 являются наиболее распространенными структурными полиморфами слоистых оксидов. Структура типа P2 имеет лучшую ионную проводимость и обеспечивает более высокую разрядную емкость, чем структура типа O3 (Qi et al., 2017). Кроме того, материал типа Р2 менее гигроскопичен, чем материал типа О3.
Оксиды переходных металлов со слоистой двумерной структурой широко изучаются из-за их улучшенных электрохимических характеристик по сравнению с другими соединениями. Эти материалы классифицируются как структуры типа O3 и P2, где буквы O и P обозначают расположение иона натрия в кристаллической структуре (P-призматическая позиция, O-октаэдрическая позиция) (рис. 1).Цифры обозначают слой переходного металла в повторяющейся элементарной ячейке структуры (Delmas, 2018). Типы O3 и P2 являются наиболее распространенными структурными полиморфами слоистых оксидов. Структура типа P2 имеет лучшую ионную проводимость и обеспечивает более высокую разрядную емкость, чем структура типа O3 (Qi et al., 2017). Кроме того, материал типа Р2 менее гигроскопичен, чем материал типа О3.
РИСУНОК 1 . Классификация слоистых материалов Na-Me-O со слоями октаэдров MeO6 с общими ребрами и процессы фазового перехода, вызванные экстракцией натрия.Перепечатано с разрешения [ref. Ябуучи и др. (2014)]. Авторское право (2014) Американское химическое общество.
(2014)]. Авторское право (2014) Американское химическое общество.
Среди материалов типа P2 катод на основе марганца (Na 2/3 MnO 2 ) привлек большое внимание из-за низкой цены на марганец и обеспечивает высокую разрядную емкость (>150 мАч·г − 1 ) по сравнению с другими исследованными катодами (Zhu et al., 2018). Однако использование марганца вызывает структурные искажения, так как в структуре преобладают ионы Mn 3+ .Это связано с ян-теллеровским искажением, состоящим из удлинения или сжатия Mn 3+ по оси z . Анизотропные изменения параметров решетки при циклировании приводят к быстрому снижению емкости (Liu et al., 2015). Одним из способов решения этой проблемы является разбавление концентрации ионов Mn 3+ в кристаллической структуре и уменьшение анизотропного изменения путем замещения его другими электрохимически активными или неактивными катионами металлов (Guo et al., 2017; Эль Моктар и др.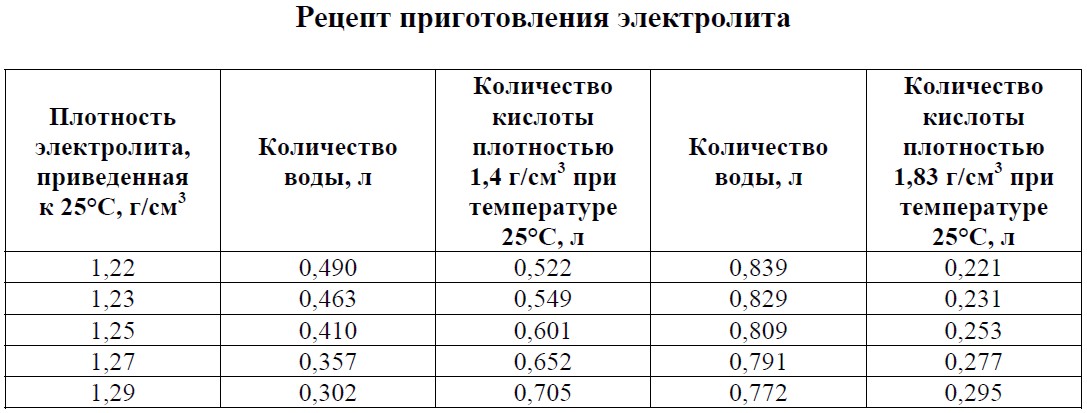 , 2018 г.; Ким и др., 2018 г.; Ирисарри и др., 2018).
, 2018 г.; Ким и др., 2018 г.; Ирисарри и др., 2018).
В этом вопросе Clément et al. (2016) изучали влияние легирования Mg на соединение Na 2/3 MnO 2 типа P2 путем изменения количества легирующей примеси: Na 2/3 Mn 1−y Mg y O 2 ( и = 0,0, 0,05, 0,1). Частичная замена Mn 3+ на Mg привела к более гладкому профилю потенциала и улучшила электрохимические характеристики композита.Успешное легирование Mg подавило ян-теллеровское искажение, что уменьшило количество Mn 3+ на Mg в P2-Na 2/3 MnO 2 . Среди составов соединение, легированное 5% Mg, показало наибольшую емкость и лучшие электрохимические свойства по сравнению с соединением с легированием 10% Mg.
Канг и др. (2015) изучали медьзамещенное соединение P2-типа Na 0,67 Cu x Mn 1–x O 2 ( x = 0, 0,14, 0,25, 0,33) для улучшения электрохимических характеристик P2 тип Na 0.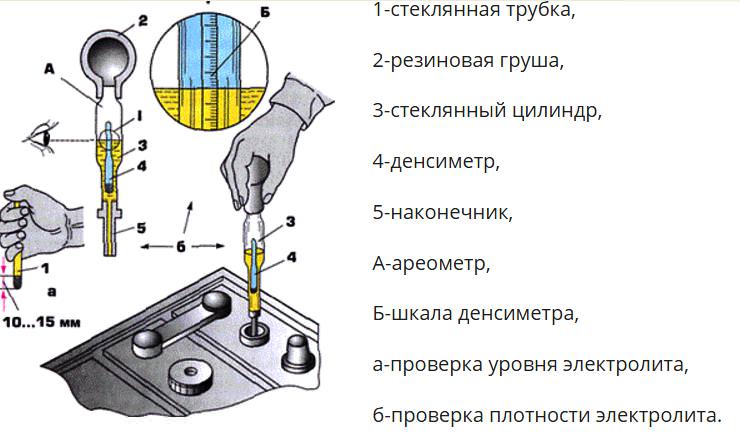 7 MnO 2 . При увеличении количества Cu в композите разрядная емкость уменьшалась. Однако реакционный потенциал увеличился за счет окислительно-восстановительной реакции Cu 2+ /Cu 3+ . В случае x = 0,25 и Mn, и Cu отвечали за обеспечение емкости. Замена части Mn 3+ на Cu привела к значительному улучшению характеристик скорости и стабильности материала.
7 MnO 2 . При увеличении количества Cu в композите разрядная емкость уменьшалась. Однако реакционный потенциал увеличился за счет окислительно-восстановительной реакции Cu 2+ /Cu 3+ . В случае x = 0,25 и Mn, и Cu отвечали за обеспечение емкости. Замена части Mn 3+ на Cu привела к значительному улучшению характеристик скорости и стабильности материала.
Lu and Dahn (2001) сообщили о замещении никелем P2-типа Na 2/3 [Mn 2/3 Ni 1/3 ]O 2 , в котором весь Mn 3+ был заменен с Ni 2+ из-за сходства размеров ионов.Композит показал высокий рабочий потенциал с окислительно-восстановительной парой Ni 2+ /Ni 4+ и обеспечил относительно высокую разрядную емкость. Кроме того, соединение продемонстрировало высокий рабочий потенциал (~3,5 В) и стабильность в водном растворе. Даже после 1 года в воде структура не сильно изменилась. Превосходные свойства соединения Na 2/3 [Mn 2/3 Ni 1/3 ]O 2 типа P2 делают его привлекательным для дальнейшей коммерциализации. Однако соединение страдало от быстрого снижения емкости; это затухание не связано с ян-теллеровским искажением из-за отсутствия Mn 3+ .Изменение фазы во время циклирования от P2 к O2 было ответственно за уменьшение емкости из-за большого изменения объема (~23%) во время фазового перехода. Было много способов решить эту проблему путем частичной замены никеля другими металлами [Mg Zheng et al. (2017), Cu Zheng et al. (2017), Zn Xu et al. (2014), Аль Хаса и др. (2017) и Li Xu et al. (2014)].
Превосходные свойства соединения Na 2/3 [Mn 2/3 Ni 1/3 ]O 2 типа P2 делают его привлекательным для дальнейшей коммерциализации. Однако соединение страдало от быстрого снижения емкости; это затухание не связано с ян-теллеровским искажением из-за отсутствия Mn 3+ .Изменение фазы во время циклирования от P2 к O2 было ответственно за уменьшение емкости из-за большого изменения объема (~23%) во время фазового перехода. Было много способов решить эту проблему путем частичной замены никеля другими металлами [Mg Zheng et al. (2017), Cu Zheng et al. (2017), Zn Xu et al. (2014), Аль Хаса и др. (2017) и Li Xu et al. (2014)].
Конаров и др. изучали Конаров и соавт. (2018) изменение содержания Ni в Р2-типе Na 2/3 Mn 1–x Ni x O 2 ( x = 0, 0.1, 0.2) для того, чтобы найти оптимальные характеристики, заключающиеся в подавлении ян-теллеровского искажения и фазового перехода от P2 к O2. Среди исследованных соединений оптимальными электрохимическими свойствами обладает Na 2/3 [Mn 0,8 Ni 0,2 ]O 2 . Соединение обеспечивало высокую емкость при высокой плотности тока (10C = 90 мА·ч·г -1 ) по сравнению с ранее сообщавшимся. Хотя во время циклирования происходила двухфазная реакция P2–O2, изменение объема составляло лишь приблизительно 10 %, что меньше, чем у Na 2/3 типа P2 [Mn 2/3 Ni 1/3 ]О 2 .
Среди исследованных соединений оптимальными электрохимическими свойствами обладает Na 2/3 [Mn 0,8 Ni 0,2 ]O 2 . Соединение обеспечивало высокую емкость при высокой плотности тока (10C = 90 мА·ч·г -1 ) по сравнению с ранее сообщавшимся. Хотя во время циклирования происходила двухфазная реакция P2–O2, изменение объема составляло лишь приблизительно 10 %, что меньше, чем у Na 2/3 типа P2 [Mn 2/3 Ni 1/3 ]О 2 .
Ортис-Виториано и др. (2017) представили доказательство концепции полных клеток с использованием слоистых оксидов натрия и марганца (Liu et al., 2015). Материал Na 0,78 Li 0,18 Ni 0,25 Mn 0,583 O w продемонстрировал электрохимические характеристики от умеренных до хороших, высокую разрядную емкость 240 г . 4,5 В, таким образом, полная плотность энергии материального уровня достигает 675 Втч·кг −1 . При циклическом изменении напряжения от 1,5 до 4,2 В разрядная емкость поддерживалась на уровне около 190 мАч·г -1 после 30 циклов.
При циклическом изменении напряжения от 1,5 до 4,2 В разрядная емкость поддерживалась на уровне около 190 мАч·г -1 после 30 циклов.
Ябуучи и др. (2014) увеличили концентрацию электрохимически неактивного Mg в P2-Na 2/3 MnO 2 до 28%, заместив почти все ионы Mn 3+ и получив Na 2/3 [Mn 0,72 Mg 0,28 ]O 2 соединение, в котором степень окисления марганца близка к 4+. Интересно, что электрохимически неактивный материал обеспечивает емкость около 150 мАч·г -1 при начальной зарядке и более 200 мАч·г -1 емкости в последующих циклах.Ожидается, что аномально большая обратимая емкость будет возникать из-за окислительно-восстановительного потенциала кислорода и активации Mn 3+ в следующих циклах, как и в катодах, богатых литием. Недавно группа Брюса изучала тот же материал (Na 2/3 [Mn 0,72 Mg 0,28 ]O 2 ) и подтвердила обратимое окислительно-восстановительное окисление кислорода в течение циклов с помощью современных инструментов (Maitra et al. , 2018). В отличие от материала с высоким содержанием лития, активация окислительно-восстановительного потенциала кислорода не требует присутствия ионов щелочных металлов в слое переходного металла.Из-за этого потеря кислорода была подавлена Mg 2+ , который связывается с кислородом, как в случае материалов с высоким содержанием лития, когда ион лития удаляется из слоя переходного металла, и это вызывает не- связанный кислород, что приводит к выделению кислорода (Maitra et al., 2018).
, 2018). В отличие от материала с высоким содержанием лития, активация окислительно-восстановительного потенциала кислорода не требует присутствия ионов щелочных металлов в слое переходного металла.Из-за этого потеря кислорода была подавлена Mg 2+ , который связывается с кислородом, как в случае материалов с высоким содержанием лития, когда ион лития удаляется из слоя переходного металла, и это вызывает не- связанный кислород, что приводит к выделению кислорода (Maitra et al., 2018).
Недавно Konarov et al. (2019) изучали эффект замещения Mn через Zn в P2-Na 2/3 Mn 1‒ x Zn x O 2 ( x = 0, 0,1, 0,1, 0,13). По мере увеличения содержания Zn емкость, генерируемая за счет окислительно-восстановительного потенциала кислорода, увеличивается. Среди различных композиций соединение P2-Na 2/3 Mn 0,7 Zn 0,3 O 2 продемонстрировало превосходные электрохимические характеристики. Существование иона Zn в слое переходного металла стабилизировало кристаллическую структуру и запускало окислительно-восстановительный процесс кислорода. В результате была поставлена разрядная емкость 190 мАч·г −1 , а после 200 циклов осталось 80%.Однако рабочий потенциал такой системы сравнительно невелик. Чтобы решить эту проблему, Ni был введен в кристаллическую структуру путем замены половины Zn в структуре (P2-Na 2/3 Mn 0,7 Zn 0,15 Ni 0,15 O 2 ). Добавление никеля привело к увеличению рабочего потенциала до 3,5 В (Конаров и др., 2020).
Существование иона Zn в слое переходного металла стабилизировало кристаллическую структуру и запускало окислительно-восстановительный процесс кислорода. В результате была поставлена разрядная емкость 190 мАч·г −1 , а после 200 циклов осталось 80%.Однако рабочий потенциал такой системы сравнительно невелик. Чтобы решить эту проблему, Ni был введен в кристаллическую структуру путем замены половины Zn в структуре (P2-Na 2/3 Mn 0,7 Zn 0,15 Ni 0,15 O 2 ). Добавление никеля привело к увеличению рабочего потенциала до 3,5 В (Конаров и др., 2020).
Среди катодов типа NASICON, показанных на рисунке 2, Na 3 V 2 (PO 4 ) 3 и его производные показали отличные электрохимические характеристики (Guo et al., 2017). Несмотря на то, что поставляемая мощность меньше, чем у слоистых оксидов, эксплуатационный потенциал делает их наиболее перспективными. Однако цена и токсичность ванадия ограничивают его дальнейшие шаги на рынке. Берлинская лазурь (PB) и ее аналоги (PBA) представляют собой большое семейство гексацианоферратов переходных металлов с открытой каркасной структурой, большим количеством окислительно-восстановительных центров и высокой структурной стабильностью. В частности, из-за их больших ионных каналов и междоузлий в решетке ПБ являются одним из немногих исходных материалов, которые могут вмещать более крупные катионы щелочных металлов, такие как ионы Na + и K + , для легких и обратимых реакций внедрения (рис. 3).Благодаря этой структурной особенности соединения ПБ интенсивно исследовались в качестве новой альтернативы и недорогого катода для введения натрия в течение последних 5 лет, хотя еще есть возможности для улучшения (Zhang, 2019). На собственные характеристики электродов из ПВА сильно влияет наличие несовершенств кристалла, таких как вакансии и молекулы воды. Увеличение вакансий увеличивает содержание координированной воды, что снижает окислительно-восстановительные центры.
Берлинская лазурь (PB) и ее аналоги (PBA) представляют собой большое семейство гексацианоферратов переходных металлов с открытой каркасной структурой, большим количеством окислительно-восстановительных центров и высокой структурной стабильностью. В частности, из-за их больших ионных каналов и междоузлий в решетке ПБ являются одним из немногих исходных материалов, которые могут вмещать более крупные катионы щелочных металлов, такие как ионы Na + и K + , для легких и обратимых реакций внедрения (рис. 3).Благодаря этой структурной особенности соединения ПБ интенсивно исследовались в качестве новой альтернативы и недорогого катода для введения натрия в течение последних 5 лет, хотя еще есть возможности для улучшения (Zhang, 2019). На собственные характеристики электродов из ПВА сильно влияет наличие несовершенств кристалла, таких как вакансии и молекулы воды. Увеличение вакансий увеличивает содержание координированной воды, что снижает окислительно-восстановительные центры. Следовательно, эти проблемы, такие как низкая разрядная емкость, низкая циклическая стабильность и низкая кулоновская эффективность, необходимо решить до коммерциализации электродов из ПВА (Wang et al., 2018).
Следовательно, эти проблемы, такие как низкая разрядная емкость, низкая циклическая стабильность и низкая кулоновская эффективность, необходимо решить до коммерциализации электродов из ПВА (Wang et al., 2018).
РИСУНОК 2 . Кристаллические структуры полианионных соединений на основе ванадия: (А) Na3V2(PO4)3 (типа НАСИКОН), (Б) Na3V2(PO4)2F3 и (В) Na7V4(P2O7)4PO4. Перепечатано с разрешения [ref. Ябуучи и др. (2014)]. Авторское право (2014) Американское химическое общество.
РИСУНОК 3 . (A) Кристаллическая структура NaxMnFe(CN)6 и (B) Электродные характеристики NaxMnFe(CN)6 в клетках Na. Перепечатано с разрешения исх.Ябуучи и др. (2014)]. Авторское право (2014) Американское химическое общество.
В различных исследованиях (You et al., 2014; Hwang et al., 2019; Chen et al., 2020) было проведено сводное исследование электрохимических характеристик различных катодных материалов. Можно провести значительное сравнение профилей заряда-разряда для этих материалов, чтобы сделать выводы о поведении катода.
Можно провести значительное сравнение профилей заряда-разряда для этих материалов, чтобы сделать выводы о поведении катода.
Типы катодов, изучаемые в этом разделе, классифицированы и сведены в таблице 1 в соответствии с их рабочими параметрами.
ТАБЛИЦА 1 . Эксплуатационные характеристики катодных материалов для органических натрий-ионных аккумуляторов.
Что касается отрицательных электродов, то в SIB можно использовать различные типы материалов, такие как материалы на основе углерода, титанаты, сплавы и оксиды/сульфиды металлов (Yu et al., 2020). Среди них материалы на основе углерода предлагают наилучшее соотношение стоимости и производительности. Джи и и др. (Hou et al., 2017) классифицировали углеродсодержащие материалы в качестве анода по четырем группам: i) графит, ii) твердый углерод, iii) углерод, легированный гетероатомами, и iv) углеродные материалы, полученные из биомассы.Обычный графитовый анод плохо работает в SIB. Из-за термодинамической нестабильности натриевого графита прогнозируется, что образование этих соединений будет стабильным только при более низких потенциалах. Поскольку графит обеспечивает небольшую емкость, твердый углерод (УВ) считается перспективным материалом из-за высокого потенциала и более широкого межслоевого расстояния, что привело к высокой обратимой емкости и отличной циклируемости (Nayak et al., 2018). Однако по-прежнему существует несколько проблем, связанных с твердым углеродом (Эль Моктар и др., 2018). Одним из них является скорость выполнения; он показывает плохую скорость из-за большого расстояния диффузии. Еще одним является низкопотенциальное плато, близкое к натриевому покрытию, которое угрожает безопасности батареи, особенно при высокой скорости. Тем не менее, некоторые недавние (Yu et al., 2020; Ma et al., 2019) исследования показали, что можно улучшить электрохимические свойства материалов этого типа с помощью методов модификации поверхности. Ван и др. показали, что углеродное нановолокно, легированное серой и азотом (SNCNF), имеет удельную емкость 247.4 мА ч г -1 (с удержанием 98,2% при 0,5 А г -1 ) в течение 600 циклов (Yu et al.
Поскольку графит обеспечивает небольшую емкость, твердый углерод (УВ) считается перспективным материалом из-за высокого потенциала и более широкого межслоевого расстояния, что привело к высокой обратимой емкости и отличной циклируемости (Nayak et al., 2018). Однако по-прежнему существует несколько проблем, связанных с твердым углеродом (Эль Моктар и др., 2018). Одним из них является скорость выполнения; он показывает плохую скорость из-за большого расстояния диффузии. Еще одним является низкопотенциальное плато, близкое к натриевому покрытию, которое угрожает безопасности батареи, особенно при высокой скорости. Тем не менее, некоторые недавние (Yu et al., 2020; Ma et al., 2019) исследования показали, что можно улучшить электрохимические свойства материалов этого типа с помощью методов модификации поверхности. Ван и др. показали, что углеродное нановолокно, легированное серой и азотом (SNCNF), имеет удельную емкость 247.4 мА ч г -1 (с удержанием 98,2% при 0,5 А г -1 ) в течение 600 циклов (Yu et al. , 2020). Хотя легирование углеродистых материалов гетероатомами способно улучшить интеркаляцию натрия, некоторые другие проблемы остаются открытыми. Ли и и др. сообщили, что легирование гетероатомами обычно приводит к более низкой внутренней кулоновской эффективности по сравнению с исходным твердым углеродом, что влияет на отношение общей стоимости к энергии разряда за срок службы (Chen et al., 2019). Поскольку экономическая конкурентоспособность действительно важна для SIB, новые конструкции анодов SIB должны соответствовать требованиям как к производительности, так и к стоимости.
, 2020). Хотя легирование углеродистых материалов гетероатомами способно улучшить интеркаляцию натрия, некоторые другие проблемы остаются открытыми. Ли и и др. сообщили, что легирование гетероатомами обычно приводит к более низкой внутренней кулоновской эффективности по сравнению с исходным твердым углеродом, что влияет на отношение общей стоимости к энергии разряда за срок службы (Chen et al., 2019). Поскольку экономическая конкурентоспособность действительно важна для SIB, новые конструкции анодов SIB должны соответствовать требованиям как к производительности, так и к стоимости.
Анализ затрат
Затраты на BESS играют важную роль, особенно для электромобилей, где стоимость аккумуляторной батареи приближается к 40–50 процентам стоимости автомобиля (Curry, 2017). Себестоимость производства зависит от многих факторов. например, материальные затраты, производственное оборудование и, если требуется, дополнительные технологии (датчики, система охлаждения, меры безопасности).
Предполагается, что в ближайшем будущем затраты на батареи на основе Na будут ниже, чем на батареи Li. Это связано не только с тем, что Na является четвертым наиболее распространенным элементом на Земле, но и с тем, что соли Na более стабильны, и их получение проще, чем получение солей Li (Zhao et al., 2017). В натрий-ионных батареях используется тот же производственный процесс, что и в LIB, и на сегодняшний день в продаже имеются натрий-ионные батареи. Благодаря использованию большого количества натрия, активных материалов, не содержащих кобальта, недорогих электролитов и имеющихся в наличии анодных материалов, SIB очень привлекательны для производителей аккумуляторов с точки зрения экономии средств. Дополнительного снижения затрат можно добиться, используя алюминиевый токосъемник вместо дорогостоящей меди, поскольку реакции сплавления между Na и Al не существует (Nayak et al., 2018).
Для получения реалистичных прогнозов стоимости расчеты должны выполняться для определенного элемента батареи с определенным значением кВтч. Поскольку натрий имеет более высокую молекулярную массу (M w ) и больший размер, чем у лития (Yabuuchi et al., 2014), теоретическая плотность энергии может снизиться, а стоимость на уровне клетки может возрасти. Еще одним фактором, влияющим на стоимость SIB, является выбор анода. Как упоминалось в предыдущем разделе, графит из традиционного анодного материала ЛИА не подходит для СИА из-за проблем интеркаляции и отсутствия стабильных соединений Na-C.В результате твердый углерод можно рассматривать как эффективный альтернативный анодный материал для SIB (El Moctar et al., 2018). Твердый углерод относительно дороже, чем обычный графитовый анод, и проблема, связанная с высокой ценой, может быть решена путем получения твердого углерода из экологически чистых и возобновляемых биоотходов. Исследователи по всему миру провели многочисленные исследования, чтобы решить упомянутые выше проблемы твердого углерода, чтобы сделать его более практичным (Kim et al., 2018; Ирисарри и др., 2018).
Поскольку натрий имеет более высокую молекулярную массу (M w ) и больший размер, чем у лития (Yabuuchi et al., 2014), теоретическая плотность энергии может снизиться, а стоимость на уровне клетки может возрасти. Еще одним фактором, влияющим на стоимость SIB, является выбор анода. Как упоминалось в предыдущем разделе, графит из традиционного анодного материала ЛИА не подходит для СИА из-за проблем интеркаляции и отсутствия стабильных соединений Na-C.В результате твердый углерод можно рассматривать как эффективный альтернативный анодный материал для SIB (El Moctar et al., 2018). Твердый углерод относительно дороже, чем обычный графитовый анод, и проблема, связанная с высокой ценой, может быть решена путем получения твердого углерода из экологически чистых и возобновляемых биоотходов. Исследователи по всему миру провели многочисленные исследования, чтобы решить упомянутые выше проблемы твердого углерода, чтобы сделать его более практичным (Kim et al., 2018; Ирисарри и др., 2018).
В настоящее время коммерческих цен на УВ кг −1 нет. Но сообщалось, что более высокая цена обусловлена дорогими прекурсорами (Kim et al., 2018). Существует множество исследований, посвященных низкозатратному синтезу УВ с высоким выходом с использованием более дешевых прекурсоров (например, целлюлозы, стеблей кукурузы, фенольной смолы) с целью оптимизации стоимости и эффективности СИБ (Irisarri et al., 2018). Бухгольц и др. использовали 15 кг −1 в качестве цены УВ; однако ее можно снизить до 8 долларов США за кг −1, , учитывая усилия, предпринимаемые для улучшения свойств твердого углерода (Vaalma et al., 2018).
Модель BatPaC Аргоннской национальной лаборатории — еще одна широко применяемая модель стоимости аккумуляторов со спецификациями для многих распространенных химических катодов, включая технологию SIB. Недавно Buchholz и соавт. представили подробный анализ затрат на SIB с использованием этой модели (Vaalma et al., 2018). Помимо материальных затрат, они приняли во внимание многие другие факторы, такие как конструкция аккумуляторной батареи (включая накладные расходы), аппаратное обеспечение, целевую мощность и энергию, чтобы рассчитать стоимость на системном уровне.
Как мы упоминали ранее, использование катодного материала, не содержащего кобальта, уже очень значительно снижает стоимость. В современной технологии ЛИА, как правило, используются катоды без кобальта (LiMn 2 O 4, LiFePO 4 ) и/или катоды с высоким содержанием никеля (NMC 532, NMC 622, NMC 811). Вот почему будущие тенденции в технологии SIB необходимо учитывать при использовании катода аналогичного типа. Если провести прямое сравнение между ЛИА и СИП с их катодами -MnO 2 , то видно, что на уровне ячейки ЛИА предлагают на 13% более дешевую стоимость, даже положительный активный материал и отрицательный токосъемник (медь) для ЛИА дороже. чем у СИБ.На системном уровне (аккумуляторная батарея 11,5 кВтч) этот ценовой разрыв уменьшается до 11 %.
Подробная стоимость материалов для LIB и SIB на основе слоистого оксидного катода, а также рассчитанная общая стоимость системы ($ кВтч −1 ), взятые из модели BatPaC, приведены на рисунке 4 и в таблице 2.
РИСУНОК 4 . Материальные затраты на литий-ионные батареи и SIB на основе слоистого оксидного катода. Данные взяты из Vaalma et al. (2018).
ТАБЛИЦА 2 . Общая стоимость системы (91 803–1 долл. США) литий-ионных аккумуляторов на основе слоистых оксидных катодов и SIB для систем мощностью 11 кВтч (Vaalma et al., 2018).
Еще одно полезное исследование было проведено Peters et al. (2017). Используя ту же модель BatPaC, они сравнили слоистый оксид (Na 1,1 Ni 0,3 Mn 0,5 Mg 0,05 Ti 0,05 O 2 ) марганцево-кобальтоксидные (Li 1,05 Ni 0,33 Mn 0,33 Co 0,33 O 2; NMC111) и литий-железо-фосфатные катоды (LiFP5 6 0 4 918).Согласно их расчетам, стоимость/кВт −1 ч составляет 263 доллара для SIB, 270 долларов для LFP и 198 долларов для NMC111. Совершенно очевидно, что SIB не могут конкурировать с LIB на основе NMC. Кроме того, следует строго учитывать, что будущие конструкции имеют тенденцию к увеличению содержания никеля в катоде (NMC622, NMC811). Поскольку кобальт является дорогостоящим сырьем, уменьшение количества кобальта автоматически снижает стоимость батареи при одновременном увеличении плотности энергии благодаря высокому содержанию никеля. В Таблице 3 приведены литературные данные по химическому составу аккумуляторов и их стоимости.
Наилучшее соотношение цена/производительность дается для усовершенствованных SIB, разработанных на основе прогнозов будущего развития. Тем не менее, цена за кВт-ч все еще намного выше, чем у литий-ионных аккумуляторов.
Помимо научных исследований, анализ рынка также подтверждает, что SIB не обеспечивают преимущества с точки зрения затрат по сравнению с LIB (Frost and Sullivan, 2019a; Frost and Sullivan, 2019b). Сообщалось, что SIB могут предложить лучшую стоимость, если только цена Li резко возрастет. Как будет обсуждаться в Резюме и Прогнозе , рост цен на литий зависит от истощения запасов, и это не произойдет в ближайшее время, вероятно, не раньше 2028 года.
Влияние Na-аккумуляторов на экономику замкнутого цикла
Доступность сырья
Литий для аккумуляторов и Na для аккумуляторов
LIB, как это прогнозируется на ближайшие годы, в основном основано на ожидаемом росте электромобильности (Graedel et al., 2015; Nassar et al., 2015; Roskill, 2019). Это привело к увеличению мощностей по добыче лития более чем в два раза с 2015 года (ок.269 000 т карбоната лития, Li 2 CO 3, эквивалент 91 806 (LCE) по сравнению с 2018 г. (около 649 000 т LCE). Хотя уровень использования в 2018 г. достиг только около 60%, ожидается, что мощности по добыче лития снова увеличатся более чем в два раза до 2024 г., достигнув примерно 1 500 000 т LCE в год (Таблица 4)
ТАБЛИЦА 4 Мощности по добыче и производству лития в отдельные годы (Roskill, 2019) прогнозируется, что спрос на литий для первого использования увеличится более чем в три раза в период с 2018 по 2023 год, достигнув 699 000 т LCE в год, мощности по добыче лития могут легко покрыть прогнозируемый спрос, вероятно, до 2025 года, согласно нашим ожиданиям (Рисунок 5).Это привело к снижению цен на Li 2 CO 3 и моногидрат гидроксида лития (LiOH) за последние 2 года, что замедляет расширение мощностей по добыче лития. Однако большинство проектов не отменяются, а откладываются, чтобы их можно было возобновить, если спрос на рынке сделает это возможным. Заглядывая дальше в будущее, до 2028 года, ожидается растущий дефицит рафинированного лития из-за дальнейшего сильного роста спроса на литий, несмотря на то, что дефицита лития в целом нет.Мировые запасы лития составляют 17 млн тонн элементарного лития (Fortier et al., 2018), что эквивалентно примерно 90 млн тонн LCE. Тем не менее, есть некоторые проблемы и риски, которые необходимо решить: i) на текущем рынке лития доминирует олигополия из пяти крупнейших производителей лития, ii) цепочка поставок лития находится под сильным влиянием китайских компаний, iii) качество аккумуляторов. Литий высокого качества представляет собой сложную задачу для производителей лития, тем более что производители должны увеличить долю лития аккумуляторного качества с примерно 40% в 2018 году до примерно 90% в 2028 году (Roskill, 2019).Достижение этой цели при условии конкурентоспособности затрат будет сложной задачей.
РИСУНОК 5 . Баланс рынка лития в 2018–2028 гг.: базовый, низкий, высокий спрос (LCE, т). Данные взяты из Ref. Роскилл (2019).
В заключение можно сказать, что лития, скорее всего, будет достаточно для удовлетворения рыночного спроса на ЛИА. Однако, если немногочисленные доступные запасы лития перейдут под контроль одного или нескольких акторов (сегодня более 70% производства литиевого сырья находится под влиянием или контролем Китая), или если нынешняя олигополия будет еще более концентрированной и находится на рассмотрении Из-за технической проблемы производства литиевого сырья для аккумуляторов производители ЛИА в некоторых странах могут столкнуться с серьезными трудностями в получении достаточного количества литиевого сырья по конкурентоспособной цене.Внедрение рентабельных технологий переработки как части экономики замкнутого цикла LIB может оказать решающее влияние на этот рынок не только с точки зрения стоимости и доступности материалов, но и с точки зрения однородного доступа к ресурсам (Graedel et al., 2011; UG Survey, 2015).
Карбонат натрия или кальцинированная сода (Na 2 CO 3 ) получают из дигидрата тринатрия гидрокарбоната (trona, Na 2 CO 3 .NaHCO 3 .2H 3 .2H
, 1996).Трона содержится в огромном количестве в морской воде (Hwang et al., 2017) и содержит более 90% смеси карбоната натрия и бикарбоната (NaHCO 3 ) (Dai and Chung, 1996). Крупнейшие в мире известные ресурсы троны находятся в Вайоминге с 47 миллиардами тонн выявленных ресурсов кальцинированной соды и. По оценкам, пласты троны во всем мире содержат около 75 миллиардов метрических тонн руды, и около 1,8 тонны троны дают 1 тонну Na 2 CO 3 (USGS National Minerals Information Center, 2020).Поскольку трона хорошо растворяется в воде, «моногидратный процесс» в основном используется для сбора Na 2 CO 3 . Solvay объявляет о своей позиции «мирового лидера» в производстве кальцинированной соды с производственной мощностью 500 тыс. тонн. Помимо троны, они также производят синтетический Na 2 CO 3 с помощью промышленного процесса, который называется «Аммиачный процесс Solvay» (Solvay). Однако этот процесс не является выгодным или благоприятным из-за его относительно высоких производственных затрат и более высокого воздействия на окружающую среду (больше выброса углекислого газа во время производства) (Национальный информационный центр по минералам Геологической службы США, 2020).
Катодные материалы
Использование материалов доминирующих в настоящее время химических элементов для литий-ионных аккумуляторов (LIB) оценивается как критическое с точки зрения риска поставок (SR). Технологии безкобальтовых аккумуляторов помимо LIB, например, Li-S или SIB, могут облегчить ситуацию с поставками будущих технологий. Риск предложения ресурсов преимущественно оценивается с помощью методологии, представленной Graedel et al. (2012) и резюмировано Бенджамином Ахзетом (2013). Анализируются различные предопределенные индикаторы, представляющие риск, связанный с будущим сокращением предложения, увеличением спроса, концентрацией рынка, а также политическими условиями в странах, занимающихся добычей полезных ископаемых.Недавняя работа Helbig et al. (2018), Венткер и соавт. (2019) применяют методологию оценки риска поставки к различным аккумуляторным технологиям. Первоначально материалы различной клеточной химии оцениваются на уровне элементов. После этого результаты агрегируются на уровне батареи на основе массы [Helbig et al. использовали различные другие методы агрегирования (Helbig et al., 2018)]. Таким образом, общий риск поставки оцененных клеточных химических веществ равен средневзвешенному значению риска поставки содержащихся материалов.В то время как Хельбиг и соавт. сосредоточиться на литий-ионных батареях, Wentker et al. включают в свою оценку различные натрий-ионные батареи (Helbig et al., 2018; Wentker et al., 2019). Тем не менее, некоторые материалы используются в обеих катодных технологиях, поэтому результаты Helbig et al. также обсуждаются в этой статье. Кроме того, проверяется, делают ли обе статьи одинаковые выводы относительно таких материалов и клеточной химии, которые оцениваются обеими.
Результаты на уровне элементов представлены в Таблице 5: В обоих исследованиях используется шкала от 0 до 100 баллов риска снабжения, где 100 баллов соответствует «наивысшему возможному риску снабжения» для оцениваемого материала.Как можно заметить, оценки риска снабжения соответствующих материалов находятся в аналогичном диапазоне. Небольшие отклонения возникают из-за различных примененных весовых коэффициентов (каждый из которых определяется в процессе аналитической иерархии) показателей и базового года используемых данных.
ТАБЛИЦА 5 . Риск поставок и ситуация со спросом/предложением различных материалов для батарей.
Хелбиг и др. сравнили различные технологии между собой, но воздержались от общих заявлений о критичности поставок.Напротив, Wentker et al. определил «порог риска предложения» в 50 пунктов. Помимо этого значения, оцениваемые материалы и технологии оцениваются как критические в отношении ситуации с их поставками. По этой классификации к критическим относятся кобальт, литий, марганец, никель, фосфор и ванадий (Helbig et al., 2018). За исключением марганца (который незначительно ниже порога критичности риска поставок, определенного ЕС) и никеля, это соответствует выводам исследования ЕС о критическом сырье (Sun et al., 2019). Градель и др. также оценивают марганец и никель как некритичные с точки зрения соответствующего риска предложения (Graedel et al., 2012). Однако необходимо отметить, что спрос на никель значительно возрастет из-за роста спроса на электромобили и одновременного более широкого применения катодов с высоким содержанием никеля. Это и потребление ресурсов другими будущими технологиями и приложениями, такими как, например, солнечные тепловые электростанции, ветряные турбины, суперсплавы и другие, потенциально могут значительно увеличить риск предложения никеля в ближайшие годы.Хелбиг и др. оценивают фосфор и марганец с более высокими баллами критичности, чем никель, в то время как это не так в оценке Wentker et al. Из оцененных материалов кобальт и литий получили самые высокие оценки риска предложения в обоих исследованиях. Напротив, натрий имеет наименьший риск поставок, за ним следует титан, который применяется в некоторых версиях SIB. Натрий в изобилии содержится в земной коре из-за его присутствия в виде различных солей в различных минералах и рассолах.
В таблице 5 также указана статическая досягаемость рассматриваемых материалов, чтобы составить представление о текущей ситуации со спросом и предложением. Ни увеличение предложения за счет переработки и разведки/экономичной добычи новых запасов, ни будущий рост спроса не учитываются индикатором статической досягаемости. Согласно этому упрощенному подходу, никель имеет самую низкую доступность материала, за ним следуют марганец и кобальт. В отличие от высокого показателя риска предложения лития, который в основном зависит от его неспособности к переработке и замене, а также от концентрации добычи в компании и стране, статический охват поставок лития очень некритичен (Sun et al., 2019). Это согласуется с выводами, обсуждаемыми в исследовании Батарея класса Li по сравнению с Аккумулятором класса Na .
В Таблице 6 представлены агрегированные результаты для риска поставок отдельных химических элементов клеток. Из технологий литий-ионных аккумуляторов Helbig et al., а также Wentker et al. оцените катод LFP с наименьшим риском подачи (хотя Helbig et al. различают LFP с анодами из графита и титаната лития) (Helbig et al., 2018; Wentker et al., 2019). Однородные результаты также можно наблюдать в отношении оценки NMC и NCA.Оба оцениваются как два наиболее важных клеточных биохимических процесса и получают одинаковые оценки риска поставок. Единственное существенное различие между двумя статьями касается химии клеток LCO. Венткер и др. оценивают ее как наиболее важную, в то время как Helbig et al. вместо этого классифицируйте риск поставки LCO среди оцененных клеточных химических реакций. Примечательно, что все технологии Na-Ion Battery оцениваются с более низкими баллами риска поставки, чем технологии Li-Ion Battery. Ни один из рассмотренных химических элементов, содержащих натрий, не превышает установленный порог критичности в 50 баллов риска снабжения.Тот факт, что NNMO и NVP оцениваются как более критические, чем NFPF и NTP, связан с риском поставок содержащихся в них никеля и ванадия. Кроме того, марганец значительно увеличивает риск поставок NNMO. Использование фосфора оказывает значительное влияние на риск поставок NFPF, NTP и NVP. Изменение химического состава элементов часто сопровождается изменениями в составе различных других компонентов аккумуляторных систем. Влияние различных материалов для анодов показано Helbig et al.для ЛФП.
ТАБЛИЦА 6 . Риск поставки различных аккумуляторных технологий/химии элементов.
Венткер и др. также оцените оценку воздействия на окружающую среду рассматриваемых клеточных химических процессов. Оценка воздействия на окружающую среду (EI) измеряется с учетом различных критериев параметров «ущерб экосистеме» и «ущерб здоровью человека». По данным Wentker et al., EI Na-Ion Technology значительно ниже, чем для преобладающих в настоящее время клеточных химических процессов (NCA, NMC).Частично это связано с использованием лития и кобальта, но в большей степени из-за воздействия производства никеля на окружающую среду (особенно в богатых никелем катодах NMC, а также NCA). Воздействие никеля в NNMO компенсируется очень низким воздействием на окружающую среду остальных катодных материалов (марганца и натрия).
Таким образом, технологии NIB более благоприятны по сравнению с технологиями LIB в отношении риска поставок содержащихся в них материалов, в основном из-за катодов, не содержащих кобальта и лития, в натрий-ионных батареях.Однако никель, который также используется в NNMO, оказывает значительное влияние на риск поставки аккумуляторных технологий. Вот почему риск поставки литий-ионных аккумуляторов с высоким содержанием никеля (например, NMC811) существенно не отличается от NMC111, хотя и сводит к минимуму количество содержащегося кобальта. Что касается материальных аспектов, то преимущество Na-Ion над Li-Ion аккумуляторами становится еще более очевидным, если принять во внимание воздействие материалов на окружающую среду (EI).
Прогноз переработки лития
Переработка использованных ЛИА является ключевым элементом для сохранения материалов в системе с замкнутым циклом, что снижает спрос на первичное сырье в производстве и потенциальный риск поставок критически важного сырья.Желательно продление срока службы LIB в приложениях второй жизни, таких как децентрализованные накопители энергии. Однако даже эти аккумуляторные системы в конечном итоге должны быть переработаны в конце их срока службы, чтобы создать экономику замкнутого цикла.
Поскольку концентрация лития в отработанных ЛИА (около 5‒7 мас.%) выше, чем в природных ресурсах, ЛИА можно рассматривать как большой запас лития (Shin et al., 2005; Yao et al., 2018 ; Лю и др., 2019). Тем не менее, основное внимание в области рециркуляции ЛИА уделяется главным образом извлечению кобальта по экономическим причинам (Liu et al., 2019). Как с экологической, так и с социально-экономической точки зрения добыча лития играет важную роль, даже если, как описано выше, запасы не закончатся до 2030 г. С одной стороны, добыча лития связана с высокими потребление воды и связанные с этим экологические последствия. С другой стороны, Европа, в частности, зависит от поставок лития из нескольких стран мира.
В целом существует два различных метода рециклинга для извлечения лития из ЛИА: пирометаллургический и гидрометаллургический методы, как показано на рисунке 6 (Mossali et al., 2020). Другие формы, такие как ремонт и регенерация катодных материалов с помощью твердофазного спекания, в данной работе не рассматриваются. Ниже кратко описаны преимущества и недостатки как методов рециркуляции, так и их технологических стадий. Особый интерес в данной работе представляет извлечение лития двумя способами рециркуляции.
Как показано на рисунке 2, использованные ЛИА разряжаются до фактической переработки, чтобы предотвратить короткое замыкание и самовозгорание аккумуляторных систем (Hanisch et al., 2015; Ли и др., 2018b; Моссали и др., 2020). Обычно это делается с использованием растворов, насыщенных солью, с тем недостатком, что литий, включенный в электролит, теряется на этом этапе процесса (Chen et al., 2019; Han et al., 2016). Без дополнительной обработки выгруженные ЛИА можно использовать в качестве сырья для пирометаллургической переработки.
Пирометаллургическая переработка является наиболее зрелой технологией переработки аккумуляторов и используется для извлечения целевых металлов при высоких температурах, что приводит к физическим и химическим превращениям.Простота операции, которую также легко масштабировать, и возможность одновременной переработки различных химических элементов аккумуляторов являются одним из основных преимуществ этого метода переработки (Baltac and Slater, 2019; Fan et al., 2020). При пирометаллургическом рециклинге ЛИА подаются в высокотемпературную шахтную печь вместе со шлакообразователем (Gaines, 2014; Harper et al., 2019). Окислительно-восстановительные реакции активируются для плавки и очистки ценных металлов (Lv et al., 2018; Zheng et al., 2018; Velázquez-Martínez et al., 2019). Выходом пирометаллургического процесса является фракция металлического сплава, содержащая, например, Ni и Co, шлак и газы (Harper et al., 2019). Чтобы избежать выброса потенциально токсичных побочных продуктов, необходимы меры по очистке газа (Gaines, 2014). Образовавшийся печной шлак состоит из золы и сгоревших компонентов, в основном содержащих алюминий, литий и другие материалы (Shin et al., 2005; Yao et al., 2018; Liu et al., 2019). Извлечение лития из шлака возможно при дальнейшей переработке в виде гидрометаллургического рециклинга (см. рис. 6).Однако это экономически невыгодно и поэтому обычно не выполняется (Gaines, 2018; Mossali et al., 2020). Вместо этого шлак можно использовать повторно, например, в качестве добавки к цементу (Gaines, 2018).
Несмотря на недостатки пирометаллургического процесса, такие как высокие капитальные затраты, образование токсичных газов, высокое потребление энергии и ограниченное количество регенерируемых материалов, пирометаллургический рециклинг остается часто используемым экономичным процессом для извлечения ценных переходных металлов. такие как кобальт и никель (Joulié et al., 2014; Гейнс, 2014; Чен и др., 2015 г.; Харпер и др., 2019 г.; Моссали и др., 2020).
Гидрометаллургическая переработка активных катодных материалов включает выщелачивание, осаждение и/или экстракцию растворителем, как показано на рис. 4 (Liu et al., 2019). Основными рабочими параметрами этого метода рециркуляции являются температура, концентрация и виды кислоты и восстановителя, время реакции и соотношение твердой и жидкой фаз (Li et al., 2018a; Harper et al., 2019; Mossali et al., 2020). В отличие от пирометаллургического рециклинга, ЛИА проходят предварительную обработку в зависимости от, например.g., клеточная химия и целевые материалы, перед их гидрометаллургической переработкой для повышения эффективности переработки (Baltac Slater, 2019; Mossali et al., 2020). Предварительная обработка включает различные процессы, такие как механическое разделение, термические процессы, процессы растворения и механохимические методы (Lv et al., 2018; Zheng et al., 2018; Mossali et al., 2020). После предварительной обработки происходит выщелачивание, т. е. растворение целевых материалов выщелачивающими реагентами. В основном выщелачивающие реагенты включают неорганические кислоты, органические кислоты и щелочные растворы (Liu et al., 2019). На выходе получается выщелачивающий раствор, содержащий такие металлы, как Ni, Co, Mn и Li. Эти металлы можно отделить от раствора путем осаждения и/или экстракции растворителем. По экономическим причинам исследования в основном были сосредоточены на выделении Ni, Co и Mn из выщелачивающего раствора, извлечение лития, напротив, имеет меньшее значение. Как показано на рисунке 7, извлечение лития в форме Li 3 PO 4 или Li 2 CO 3 обычно является одним из последних процессов.(Лю и др., 2019). Поскольку потери лития неизбежны и накапливаются при выделении Ni, Co и Mn из выщелачивающего раствора, эффективность рециркуляции лития зависит от предшествующих технологических стадий.
РИСУНОК 7 . Восстановление активных катодных материалов из литий-ионных аккумуляторов (Liu et al., 2019).
В целом основными преимуществами гидрометаллургических процессов по сравнению с пирометаллургическими являются более высокая эффективность извлечения ценных металлов, особенно лития, более низкое потребление энергии, меньшее образование токсичных газов и более низкие капитальные затраты (Lv et al., 2018; Фан и др., 2020 г.; Моссали и др., 2020). Основными недостатками использования гидрометаллургических процессов для переработки литий-ионных аккумуляторов являются высокая зависимость от предварительной обработки и используемых технологий, выбросы, связанные с используемыми химическими веществами, и сложность одновременной обработки различных химических элементов аккумуляторов (Baltac and Slater, 2019; Mossali et al., 2020). ). Это связано с тем, что каждая последовательность переработки должна быть оптимизирована для определенного химического состава батареи, чтобы обеспечить высокую степень извлечения материалов и выгодную экономику (Baltac and Slater, 2019).Гидрометаллургическая переработка обеспечивает степень извлечения около 95% Ni и Co в виде солей, в то время как Cu может быть извлечена до 100%, а Li — около 90%. Для достижения таких высоких скоростей процессы выщелачивания обычно адаптируются к конкретному химическому составу аккумуляторов, и необходимы обширные процессы предварительной обработки. При использовании гидрометаллургической переработки после пирометаллургического процесса возможно дорогостоящее извлечение около 50–60% лития (Fan et al., 2020; Frost and Sullivan, 2020). В будущем процессы гидрометаллургической переработки потребуют эффективного и более быстрого удаления примесей для повышения чистоты восстановленных материалов (Fan et al., 2020; Фрост и Салливан, 2020 г.). Кроме того, новые комбинации пирометаллургической переработки при более низких температурах и бескислотной/щелочной гидрометаллургической переработки, такие как вакуумное карботермическое восстановление и сульфатный обжиг, кажутся многообещающими и требуют будущих исследований и промышленного внедрения (Liu et al., 2019).
Исследование Liu et al. показывает, что извлечение лития в промышленных масштабах до сих пор играло лишь незначительную роль. В настоящее время только два из четырнадцати проанализированных процессов переработки литий-ионных аккумуляторов от разных компаний извлекают литий (Liu et al., 2019). С экономической точки зрения извлечение лития в настоящее время нецелесообразно. Вместо этого основное внимание уделяется извлечению более дорогих металлов: кобальта, никеля (Swain, 2017).
Было найдено мало информации о стратегиях утилизации SIB. Это связано с отсутствием соответствующего количества аккумуляторов EoL-Na-Ion. Тем не менее, одной из задач текущего проекта NAIMA является разработка «устойчивого и экономически эффективного процесса переработки вторичных вторсырьев» (European Comission, 2019).Кроме того, Ассоциация европейских производителей автомобильных и промышленных аккумуляторов описывает хлоридно-натриевые аккумуляторы как «полностью пригодные для вторичной переработки в существующих отраслях производства нержавеющей стали и дорожного покрытия» (Ассоциация европейских производителей автомобильных и промышленных аккумуляторов). Хотя только в лабораторных масштабах, Liu et al. недавно разработали конструкцию для переработки натрий-ионных аккумуляторов. Переработка этой батареи привела к эффективности переработки твердых компонентов более 98% (Liu et al., 1965). Фаза дизайна продукта также выделяется Hirsh et al. Поскольку производители для SIB только начинают масштабировать свое производство, ожидается, что они будут более гибкими в использовании методов устойчивого проектирования продуктов, чем известные производители LIB. Кроме того, прослеживаемость состава материалов рассматривается как важный аспект будущей переработки СИБ. Потребность в передаче информации по всей цепочке поставок усиливается в связи с ожидаемым основным применением СИБ в качестве стационарных аккумуляторных батарей и связанным с этим сроком службы (Hirsh et al., 2020).
Резюме и перспективы
Хотя технология SIB и ее производство уже находятся на уровне коммерциализации, до сих пор она нашла мало возможностей для коммерческого применения. SIB используют тот же производственный процесс, что и LIB, что является большим преимуществом для производителей. Экономические преимущества SIB заключаются в экологичных и дешевых катодных материалах (NaCO 3 , активные материалы, не содержащие кобальта), а также в использовании алюминиевых токосъемников как для отрицательного, так и для положительного электродов.Однако, как объяснялось в предыдущих главах, этих преимуществ недостаточно для снижения стоимости батареи. Кроме того, удельная энергетическая плотность современных СИП также не выше, чем у ЛИА.
Инновационная стратегия дизайна элементов для этих батарей необходима для баланса между высокой плотностью энергии и снижением общей стоимости батареи. Согласно рыночным отчетам, технология SIB может выйти на более конкурентоспособный уровень после 2025 года, особенно для крупномасштабных систем хранения энергии.
После 2025 года требуемая емкость аккумуляторов для рынка электромобилей составляет 1559 ГВтч (Automotive Competence Center & Forschungsgesellschaft Kraftwahrwesen mbH Aachen, 2018).В результате после 2028 года ожидается растущий дефицит рафинированного лития из-за дальнейшего сильного роста спроса на литий. Этот спрос будет в основном состоять из лития аккумуляторного качества, доля которого, как ожидается, увеличится с 40% в 2018 году до примерно 90% в 2028 году. Достижение этой цели в условиях конкурентоспособности затрат будет сложной задачей. Это означает, что использование SIB параллельно с LIB для стационарных и краткосрочных электромобильных приложений (электровелосипеды, электронные скутеры) определенно снизит нагрузку на цепочку поставок лития.
Кроме того, современная технология переработки лития является очень дорогостоящей, и затраты на производство батарей должны включать расходы на переработку. До сих пор таких исследований затрат на рециркуляцию не проводилось. И последнее, но не менее важное: известно, что электромобиль с технологией LIB производит больше выбросов CO 2 во время производства, чем транспортное средство с двигателем внутреннего сгорания, из-за очень энергоемкого производства LIB и их сырья, такого как аккумуляторная батарея. литий. Поскольку натрий для аккумуляторов может быть извлечен из морской воды и произведен относительно легче, чем литий, эти батареи можно считать более безопасными для окружающей среды.
Нет сомнений в том, что конкуренция между LIB и SIB будет продолжаться. Тем не менее, основное продвижение к SIB будет достигнуто за счет внедрения новых экономичных материалов и новых концепций ячеек.
Вклад авторов
Авторы подтверждают вклад в статью следующим образом: концепция и дизайн исследования: DK, KB и ZB; сбор данных, анализ и интерпретация результатов, а также подготовка проекта рукописи: DK, SS, SK, JK, AK, FS, RM, MW, ZB и KB.Все авторы рассмотрели результаты и одобрили окончательный вариант рукописи.
Конфликт интересов
Авторы заявляют, что исследование проводилось при отсутствии каких-либо коммерческих или финансовых отношений, которые могли бы быть истолкованы как потенциальный конфликт интересов.
Благодарности
Это исследование было проведено в рамках проекта «DigiBattPro 4.0 BW». Авторы выражают благодарность Министерству экономики, труда и жилищного строительства земли Баден-Вюртемберг за финансовую поддержку.
Ссылки
Адельхельм П., Хартманн П., Бендер К.Л., Буше М., Эуфингер К. и Янек Дж. (2015). От лития к натрию: клеточная химия натрий-воздушных и натрий-серных батарей комнатной температуры. Beilstein J. Nanotechnol. 6, 1016–1055. doi:10.3762/bjnano.6.105
Полный текст CrossRef | Google Scholar
Ахмади Л., Янг С. Б., Фаулер М., Фрейзер Р. А. и Ачахлуи М. А. (2017). Каскадный жизненный цикл: повторное использование литий-ионных аккумуляторных батарей электромобилей в системах накопления энергии. Междунар. J. Оценка жизненного цикла. 22 (1), 111–124. doi:10.1007/s11367-015-0959-7
Полный текст CrossRef | Google Scholar
Аль-Тиабат С., Накамура Т., Шибата Э. и Иидзука А. (2013). Адаптация операций по переработке полезных ископаемых для переработки литий-ионных (LiB) и никель-металлогидридных (NiMH) аккумуляторов: критический обзор. Шахтер. англ. 45, 4–17. doi:10.1016/j.mineng.2012.12.005
Полный текст CrossRef | Google Scholar
Эмброуз Х. и Кендалл А.(2020а). Понимание будущего лития: Часть 1, ресурсная модель. J. Ind. Ecol. 24 (1), 80–89. doi:10.1111/jiec.12949
Полный текст CrossRef | Google Scholar
Амброуз Х. и Кендалл А. (2020b). Понимание будущего лития: Часть 2, моделирование оценки жизненного цикла с временным и пространственным разрешением. J. Ind. Ecol. 24 (1), 90–100. doi:10.1111/jiec.12942
Полный текст CrossRef | Google Scholar
Automotive Competence Center & Forschungsgesellschaft Kraftwahrwesen mbH Aachen (2018). Индекс электромобильности 2018 . Роланд Бергер.
Google Scholar
Балтак С. и Слейтер С. (2019). Аккумуляторы на колесах: роль аккумуляторных электромобилей в энергосистеме ЕС и за его пределами. Энергия элемента.
Google Scholar
Баркер, Дж. (2017). «Прогресс в коммерциализации технологии ионно-натриевых батарей Фарадиона», 4-я международная конференция по натриевым батареям, Токио, Япония, 28–30 ноября 2017 г.
Google Scholar
Bauer, A., Сонг Дж., Вейл С., Пан В., Баркер Дж. и Лу Ю. (2018). Масштабирование и коммерциализация технологий неводных натрий-ионных аккумуляторов. Доп. Энергия Матер. 8 (17), 1702869. doi:10.1002/aenm.201702869
CrossRef Полный текст | Google Scholar
Benjamin Achzet, CH (2013). «Как оценить риски поставок сырья — обзор. Ресурс. пол. 38 (4), 435–447. doi:10.1016/j.resourpol.2013.06.003
CrossRef Полный текст | Google Scholar
Бин, Д., Wang, F., Tamirat, A.G., Suo, L., Wang, Y., Wang, C., et al. (2018). Прогресс в водных перезаряжаемых натрий-ионных батареях. Доп. Энергия Матер. 8 (17), 1703008. doi:10.1002/aenm.201703008
CrossRef Полный текст | Google Scholar
Чен М., Корти Д., Ху З., Джин Х., Ван С., Гу Q. и др. (2018). Новый катодный композит Na 2 Fe 2 (SO 4 ) 3/C с оболочкой из оксида графена для долговечных и высокоплотных натрий-ионных аккумуляторов. Доп. Энергия Матер. 8 (27), 1800944.doi:10.1002/aenm.201800944
Полный текст CrossRef | Google Scholar
Чен М., Хуа В., Сяо Дж., Корти Д., Чен В., Ван Э., Ху З. и др. (2019). Воздухостабильный и всеклиматический катод типа NASICON для натрий-ионных аккумуляторов с низкой стоимостью и высокой удельной мощностью. Нац. коммун. 10 (1), 1–11. doi:10.1038/s41467-019-09170-5
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Чен М., Чжан Ю., Син Г. и Тан Ю. (2020). Создание высокой удельной мощности натрий-ионных аккумуляторов: важность путей многомерной диффузии в катодных материалах. Фронт. хим. 8, 152. doi:10.3389/fchem.2020.00152
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Чен Т., Джин Ю., Лв Х., Ян А., Лю М., Чен Б. и др. (2020). Применение литий-ионных аккумуляторов в сетевых системах хранения энергии. Пер. Тяньцзиньский унив. 26 (3), 208–217. doi:10.1007/s12209-020-00236-w
CrossRef Full Text | Google Scholar
Чен X., Чен Ю., Чжоу Т., Лю Д., Ху Х. и Фань С. (2015).Гидрометаллургическое извлечение металлов из сернокислотного выщелачивания отработанных литий-ионных аккумуляторов. Управление отходами. 38, 349–356. doi:10.1016/j.wasman.2014.12.023
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Чен С., Чжэн Ю., Лю В., Чжан С., Ли С. и Ли Дж. (2019). «Высокоэффективные натрий-ионные аккумуляторы с твердым углеродным анодом: переход от полуэлемента к полноэлементу. Наношкала 11 (46), 22196–22205. дои: 10.1039/C9NR07545C
Реферат PubMed | Полный текст перекрестной ссылки | Google Scholar
Клеман Р. Дж., Бийо Ф., Армстронг А. Р., Сингх Г., Рохо Т., Брюсебд П. Г. и др. (2016). Структурно стабильные натрий-ионные аккумуляторные катоды P2-Na2/3Mn1-yMgyO2, легированные магнием, с высокой производительностью: результаты электрохимических, ЯМР и дифракционных исследований. Энергетическая среда. науч. 9 (10), 3240–3251. doi:10.1039/C6EE01750A
Полный текст CrossRef | Google Scholar
Карри, К.(2017). Стоимость и рынок литий-ионных аккумуляторов . Bloomberg-Новые энергетические финансы.
Google Scholar
Дай К. и Чанг К. Х. (1996). Карбонат натрия минерального качества Trona в качестве технологической добавки для процесса горячей воды. Дж. Кан. Бензин. Технол. 35 (1). doi:10.2118/96-01-08
Полный текст CrossRef | Google Scholar
Дельмас, К. (2018). Натриевые и натрий-ионные батареи: 50 лет исследований. Доп. Энергия Матер. 8 (17), 1703137.doi:10.1002/aenm.201703137
Полный текст CrossRef | Google Scholar
Дэн Дж., Луо В. Б., Лу X., Яо К., Ван З., Лю Х. К. и др. (2018). Натрий-ионный аккумулятор с высокой плотностью энергии и стабильным на воздухе многослойным оксидным катодом типа O3. Доп. Энергетический материал. 8 (5), 1701610. doi:10.1002/aenm.201701610
CrossRef Полный текст | Google Scholar
Дин Ю., Кано З. П., Ю А., Лу Дж. и Чен З. (2019). Автомобильные литий-ионные аккумуляторы: текущее состояние и перспективы на будущее. Электрохим. Энерг. 2 (1), 1–28. doi:10.1007/s41918-018-0022-z
Полный текст CrossRef | Google Scholar
Долега П. (2019). Gigafactories für Lithium-Ionen-Zellen, Rohstoffbedarfe für die Globale Elektromobilität bis 2050 . Дармштадт: Öko-Institut e-V.
Google Scholar
Эль Моктар И., Ни К., Бай Ю., Ву Ф. и Ву К. (2018). Твердые углеродные анодные материалы для натрий-ионных аккумуляторов. Функц. Матер. лат. 11 (6), 1830003.doi:10.1142/S1793604718300037
Полный текст CrossRef | Google Scholar
Эллис Б.Л. и Назар Л.Ф. (2012). Натриевые и натрий-ионные аккумуляторные батареи. Курс. мнение Твердотельный материал. науч. 16 (4), 168–177. doi:10.1016/j.cossms.2012.04.002
Полный текст CrossRef | Google Scholar
Этачери В., Маром Р., Элазари Р., Салитра Г. и Аурбах Д. (2011). Проблемы разработки перспективных литий-ионных аккумуляторов: обзор. Энергетическая среда.науч. 4 (9), 3243. doi:10.1039/c1ee01598b
CrossRef Full Text | Google Scholar
Юхнер, Х., Клеменс, О., и Редди, Массачусетс (2019). Раскрытие потенциала фторидов металлов типа веберита в электрохимическом накоплении энергии. Npj Comput Mater 5 (1), 1–10. doi:10.1038/s41524-019-0166-3
CrossRef Full Text | Google Scholar
Fan, E., Li, L., Wang, Z., Lin, J., Huang, Y., Yao, Y., et al. (2020). Устойчивая технология переработки литий-ионных аккумуляторов и не только: проблемы и перспективы на будущее. Хим. Ред. 120 (14), 7020–7063. doi:10.1021/acs.chemrev.9b00535
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Fortier, S.M., Hammarstrom, JH, Ryker, SJ, Day, WC, and Seal, R.R. (2018). Геологическая служба США, 806 «Горное дело, 2019-USGS Critical Minerals Review. Министерство торговли США .
Google Scholar
Фрост и Салливан (2019a). Прорывные технологии хранения аккумуляторов: ожидается, что в следующем десятилетии новые аккумуляторные технологии, помимо химии литий-иона, произведут переворот на рынке аккумуляторов .Санта-Клара: Фрост и Салливан.
Google Scholar
Фрост и Салливан (2019b). Мировой рынок литий-ионных аккумуляторов, прогноз до 2025 г. . Санта-Клара: Фрост и Салливан.
Google Scholar
Фрост и Салливан (2020). Утилизация литий-ионных аккумуляторов с истекшим сроком службы: технологии переработки аккумуляторов: инновационные технологии восстановления и повторного использования ценных металлов из литий-ионных аккумуляторов с истекшим сроком службы . Д952-ТВ.
Google Scholar
Гейнс, Л.(2014). Будущее утилизации автомобильных литий-ионных аккумуляторов: наметить устойчивый курс. Устойчивый материал. Техноло. 1–2, 2–7. doi:10.1016/j.susmat.2014.10.001
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Гейнс, Л. (2018). Процессы переработки литий-ионных аккумуляторов: исследования в направлении устойчивого развития. Устойчивый материал. Технол. 17, e00068. doi:10.1016/j.susmat.2018.e00068
Полный текст CrossRef | Google Scholar
Градель, Т.E., Allwood, J., Birat, J.-P., Reck, B.K., Sibley, S.F., Sonnemann, G., et al. (2011). ЮНЕП (2011 г.) Темпы переработки металлов – отчет о состоянии, Отчет рабочей группы по глобальным потокам металлов для международной группы ресурсов .
Google Scholar
Градель, Т. Э., Барр, Р., Чендлер, К., Чейз, Т., Чой, Дж., Кристоферсен, Л., и др. (2012). Методика определения критичности металлов. Окружающая среда. науч. Технол. 46 (2), 1063–1070. дои: 10.1021/es203534z
Реферат PubMed | Полный текст перекрестной ссылки | Google Scholar
Гредель, Т. Е., Харпер, Э. М., Нассар, Н. Т., и Рек, Б. К. (2015). На материальной базе современного общества. Проц. Натл. акад. науч. США 112 (20), 6295–6300. doi:10.1073/pnas.1312752110
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Guo, J.-Z., Wang, P.F., Wu, X.L., Zhang, X.H., Yan, Q., Chen, H., et al. (2017). Высокоэнергетический/мощный и низкотемпературный катод для натрий-ионных аккумуляторов: рентгенографическое исследование in situ и превосходные характеристики полноэлементных элементов. Доп. Материал. (Дирфилд-Бич, Флорида) 29, 33. doi:10.1002/adma.201701968
CrossRef Полный текст | Google Scholar
Guo, S., Yu, H., Jian, Z., Liu, P., Zhu, Y., Guo, X., et al. (2014). Высокоемкий недорогой слоистый оксид натрия-марганца в качестве катода для натрий-ионных аккумуляторов. ChemSusChem 7 (8), 2115–2119. doi:10.1002/cssc.201402138
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Хабиб А. и Соу К. (2018).Аналитический обзор тенденций и текущего состояния крупномасштабных устойчивых технологий хранения энергии. евро. Дж. Устойчивое развитие. Рез. 2 (3). doi:10.20897/ejosdr/86200
Полный текст CrossRef | Google Scholar
Хан, М. Х., Гонсало, Э., Шарма, Н., Лопес дель Амо, Дж. М., Арманд, М., Авдеев, М., и др. (2016). Высокоэффективный катодный материал P2-фазы Na 2/3 Mn 0,8 Fe 0,1 Ti 0,1 O 2 для натрий-ионных аккумуляторов, работающих при температуре окружающей среды. Хим. Матер. 28 (1), 106–116.doi:10.1021/acs.chemmater.5b03276
Полный текст CrossRef | Google Scholar
Ханиш К., Лельхоффель Т., Дикманн Дж., Маркли К. Дж., Хазелридер В. и Кваде А. (2015). Переработка литий-ионных аккумуляторов: новый метод разделения покрытия и фольги электродов. Дж. Чистый. Произв. 108, 301–311. doi:10.1016/j.jclepro.2015.08.026
Полный текст CrossRef | Google Scholar
Харпер Г., Соммервиль Р., Кендрик Э., Дрисколл Л., Слейтер П., Столкин Р., и другие. (2019). Переработка литий-ионных аккумуляторов от электромобилей. Природа 575 (7781), 75–86. doi:10.1038/s41586-019-1682-5
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Хаса И., Пассерини С. и Хассун Дж. (2017). К катодным материалам с высокой плотностью энергии для натрий-ионных аккумуляторов: исследование положительного влияния легирования алюминием на структуру типа P2. Дж. Матер. хим. 5 (9), 4467–4477. doi:10.1039/C6TA08667E
Полный текст перекрестной ссылки | Google Scholar
Хельбиг, К., Брэдшоу А.М., Витчел Л., Торенц А. и Тума А. (2018). Риски поставок, связанные с материалами для литий-ионных аккумуляторов. Дж. Чистый. Произв. 172, 274–286. doi:10.1016/j.jclepro.2017.10.122
Полный текст CrossRef | Google Scholar
Хирш Х.С., Ли Ю., Тан Д.Х.С., Чжан М., Чжао Э. и Мэн Ю.С. (2020). Натрий-ионные аккумуляторы прокладывают путь к накоплению энергии в сети. Доп. Энергетический материал. 10, 32. doi:10.1002/AENM.22001274
CrossRef Full Text | Google Scholar
Хоу, Х., Qiu, X., Wei, W., Zhang, Y., and Ji, X. (2017). Углеродные анодные материалы для современных натрий-ионных аккумуляторов. Доп. Энергия Матер. 7 (24), 1602898. doi:10.1002/aenm.201602898
CrossRef Полный текст | Google Scholar
Хван Дж.-Ю., Ким Дж., Ю Т.-Ю. и Сун Ю.-К. (2019). «Новый слоистый оксидный катод типа P2 с чрезвычайно высокой плотностью энергии для натрий-ионных аккумуляторов. Доп. Энергия Матер. 9 (15), 1803346. doi:10.1002/aenm.201803346
CrossRef Полный текст | Google Scholar
Ирисарри Э., Tennison, S., Ghimbeu, C., Gorka, J., Vix, C., Ponrouch, A., et al. (2018). Оптимизация характеристик крупномасштабного производства твердого углерода в натрий-ионных батареях: влияние прекурсора, температуры и условий обработки. Дж. Электрохим. соц. 165 (16), А4058–А4066. doi:10.1149/2.1171816jes
CrossRef Full Text | Google Scholar
Жулье М., Локурне Р. и Билли Э. (2014). Гидрометаллургический процесс восстановления ценных металлов из отработанных литий-ионных аккумуляторов на основе литий-никель-кобальт-алюминий-оксид. Дж. Источники питания 247, 551–555. doi:10.1016/j.jpowsour.2013.08.128
CrossRef Полный текст | Google Scholar
Канг В., Чжан З., Ли П.К., Нг, Т.В., Ли В., Тан Ю. и др. (2015). Замещенный медью P2-тип Na0,67CuxMn1−xO2: стабильный мощный катод для натрий-ионного аккумулятора. Дж. Матер. хим. 3 (45), 22846–22852. doi:10.1039/C5TA06371J
CrossRef Полный текст | Google Scholar
Ким Х., Эон Квон Дж., Ли Б., Хонг Дж., Ли М., Янг Парк С., и другие. (2015). Высокоэнергетический органический катод для натриевых аккумуляторов. Хим. Матер. 27 (21), 7258–7264. doi:10.1021/acs.chemmater.5b02569
Полный текст CrossRef | Google Scholar
Ким Ю., Ким Дж.-К., Ваалма К., Бэ Г.Х., Ким Г.-Т., Пассерини С. и Ким Ю. (2018). Оптимизированный твердый углерод, полученный из крахмала, для перезаряжаемых аккумуляторов с морской водой. Углерод 129, 564–571. doi:10.1016/j.carbon.2017.12.059
CrossRef Полный текст | Google Scholar
Конаров А., Чой, Дж. У., Бакенов, З., и Мён, С.-Т. (2018). Пересмотр слоистых оксидов натрия-марганца: достижение высокой энергии за счет включения Ni. Дж. Матер. хим. 6 (18), 8558–8567. doi:10.1039/C8TA02067A
Полный текст CrossRef | Google Scholar
Конаров А., Джэ Ким Х., Джо Дж. Х., Воронина Н., Ли Ю., Бакенов З. и др. (2020). Высоковольтный кислородно-окислительно-восстановительный катод для перезаряжаемых натрий-ионных аккумуляторов. Доп. Энергия Матер. 10 (24), 2001111. doi:10.1002/aenm.202001111
CrossRef Полный текст | Google Scholar
Конаров А., Джо Дж. Х., Чой Дж. У., Бакенов З., Яширо Х., Ким Дж., Мён С.-Т. (2019). Исключительно высокостабильная производительность при циклировании и легкий окислительно-восстановительный потенциал катодных материалов на основе марганца для перезаряжаемых натриевых батарей. Наноматер. Энергия 59, 197–206. doi:10.1016/j.nanoen.2019.02.042
Полный текст CrossRef | Google Scholar
Ланда-Медрано И., Ли К., Ортис-Виториано Н., Руис де Ларраменди, И., Карраско, Дж., и Рохо, Т. (2016). Натрий-кислородная батарея: шаги к реальности. J. Phys. хим. лат. 7 (7), 1161–1166. doi:10.1021/acs.jpclett.5b02845
Полный текст CrossRef | Google Scholar
Li, L., Biana, Y., Zhanga, X., Guanc, Y., Fana, E., Wu, F., et al. (2018а). Процесс переработки материалов смешанного катода из отработанных литий-ионных аккумуляторов и кинетика выщелачивания. Управление отходами. 71, 362–371. doi:10.1016/j.wasman.2017.10.028
Полнотекстовая перекрестная ссылка | Google Scholar
Li, L., Li, L., Zhang, X., Li, M., Chen, R., Wu, F., et al. (2018б). Переработка отработанных литий-ионных аккумуляторов: обзор современных процессов и технологий. Электрохим. Энерг. Ред. 1 (4), 461–482. doi:10.1007/s41918-018-0012-1
Полный текст CrossRef | Google Scholar
Ли Л., Лу Ю., Чжан К., Чжао С., Ху З. и Чоу С.-Л. (2019). Недавний прогресс в области слоистых катодных материалов для неводных перезаряжаемых магниевых батарей. Маленький e1
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Лю Б., Чжан Дж.-Г. и Сюй В. (2018). Продвижение литий-металлических батарей. Дж 2 (5), 833–845. doi:10.1016/j.joule.2018.03.008
Полный текст CrossRef | Google Scholar
Лю К., Линь Дж., Цао Х., Чжан Ю. и Сунь З. (2019). Переработка отработанных литий-ионных аккумуляторов с учетом восстановления лития: критический обзор. Дж.Чистый. Произв. 228, 801–813. doi:10.1016/j.jclepro.2019.04.304
Полный текст CrossRef | Google Scholar
Лю Х., Сюй Дж., Ма К. и Мэн Ю. С. (2015). Новый слоистый оксидный катод типа O3 с высокой плотностью энергии/мощности для перезаряжаемых Na-батарей. Хим. коммун. 51 (22), 4693–4696. doi:10.1039/c4cc09760b
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Лю Т., Чжан Ю., Чен С., Линь З., Чжан С. и Лу Дж. (1965). Полностью перерабатываемый натрий-ионный аккумулятор, основанный на принципах устойчивого развития. Нац. коммун. 10, 1. doi:10.1038/s41467-019-09933-0
CrossRef Full Text | Google Scholar
Лю Ю., Хе П. и Чжоу Х. (2018). Перезаряжаемые твердотельные Li-air и Li-S батареи: материалы, конструкция и проблемы. Доп. Энергия Матер. 8 (4), 1701602. doi:10.1002/aenm.201701602
CrossRef Полный текст | Google Scholar
Лу З. и Дан Дж. Р. (2001). I n situ Рентгеноструктурное исследование P 2 Na2/3 [Ni1/3Mn2/3] O 2 . Дж. Электрохим. соц. 148, 11. doi:10.1149/1.1407247.A1225
CrossRef Полный текст | Google Scholar
Луо Дж., Сунь С., Пэн Дж., Лю Б., Хуанг Ю., Ван К. и др. (2017). Наносферы берлинской лазури, обернутые графеновым валиком, в качестве высокоэффективного катода без связующего вещества для натрий-ионных аккумуляторов. Приложение ACS Матер. Интерфейсы 9 (30), 25317–25322. doi:10.1021/acsami.7b06334
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Lv, W., Wang, Z., Цао Х., Сунь Ю., Чжан Ю. и Сунь З. (2018). Критический обзор и анализ утилизации отработанных литий-ионных аккумуляторов. ACS Sustain. хим. англ. 6 (2), 1504–1521. doi:10.1021/acssuschemeng.7b03811
Полный текст CrossRef | Google Scholar
Ma, X., Xiong, X., Zou, P., Liu, W., Wang, F., Liang, X., et al. (2019). «Общее и масштабируемое производство сульфидов металлов @ C с ядром и оболочкой, закрепленных на трехмерной пене, легированной азотом, для гибких натрий-ионных батарей. Маленький 15–45.doi:10.1002/smll.2019
Полный текст CrossRef | Google Scholar
MacLaughlin, CM (2019). Состояние и перспективы технологий магниевых аккумуляторов: беседа со Стэном Уиттингемом и Сарбаджитом Банерджи. ACS Energy Письмо. 4 (2), 572–575. doi:10.1021/acsenergylett.9b00214
Полный текст CrossRef | Google Scholar
Майтра У., Хаус Р. А., Сомервилль Дж. В., Тапиа-Руис Н., Лозано Дж. Г., Геррини Н. и др. (2018). Окислительно-восстановительная химия без избытка ионов щелочных металлов в Na2/3Mg0.28Mn0,72O2. Нац. хим. 10 (3), 288–295. doi:10.1038/nchem.2923
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Мао М., Луо К., Поллард Т. П., Хоу С., Гао Т., Фань X., Цуй К. и др. (2019). Полимер на основе пиразина для быстрозаряжаемых аккумуляторов. Анжю. хим. 58 (49), 17820–17826. doi:10.1002/anie.2016
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Мин Дж., Го Дж., Ся К., Ван В. и Альшариф Х.Н. (2019). Цинк-ионные аккумуляторы: материалы, механизмы и применение. Матер. науч. англ. R. Rep. 135, 58–84. doi:10.1016/j.mser.2018.10.002
Полный текст CrossRef | Google Scholar
Моссали Э., Пиконе Н., Джентилини Л., Родригес О., Перес Дж. М. и Колледани М. (2020). Литий-ионные батареи на пути к экономике замкнутого цикла: обзор литературы о возможностях и проблемах переработки. Дж. Окружающая среда. Управление 264, 110500. doi:10.1016/j.jenvman.2020.110500
Полнотекстовая перекрестная ссылка | Google Scholar
Нассар, Н. Т., Градель, Т. Е., и Харпер, Э. М. (2015). Побочные металлы необходимы с технологической точки зрения, но их поставка проблематична. Науч. Доп. 1 (3), е1400180. doi:10.1126/sciadv.1400180
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Наяк П.К., Ян Л., Брем В. и Адельхельм П. (2018). От литий-ионных к натрий-ионным батареям: преимущества, проблемы и неожиданности. Анжю.хим. 57 (1), 102–120. doi:10.1002/anie.201703772
Полный текст CrossRef | Google Scholar
Ортис-Виториано, Н., Древетт, Н. Э., Гонсало, Э., и Рохо, Т. (2017). Высокоэффективные слоистые оксидные катоды на основе марганца: преодоление проблем, связанных с натрий-ионными батареями. Энергетическая среда. науч. 10 (5), 1051–1074. doi:10.1039/C7EE00566K
Полный текст перекрестной ссылки | Google Scholar
Осима Т., Кадзита М. и Окуно А. (2004). «Разработка натрий-серных аккумуляторов. Междунар. Дж. Заявл. Керам. Технол. 1 (3), 269–276. doi:10.1111/j.1744-7402.2004.tb00179.x
Полный текст CrossRef | Google Scholar
Пэн Ф., Ю Л., Юань С., Ляо X. Z., Вэнь Дж., Тан Г. и др. (2019). Улучшенные электрохимические характеристики ферроцианида натрия-марганца за счет покрытия Na3(VOPO4)2F для натрий-ионных аккумуляторов. Приложение ACS Матер. Интерфейсы 11 (41), 37685–37692. doi:10.1021/acsami.9b12041
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Питерс Дж.Ф., Бауманн М., Циммерманн Б., Браун Дж. и Вейл М. (2017). Воздействие литий-ионных аккумуляторов на окружающую среду и роль ключевых параметров — обзор. Продлить. Поддерживать. Energy Rev. 67, 491–506. doi:10.1016/j.rser.2016.08.039
Полный текст CrossRef | Google Scholar
Понроуч А., Монти Д., Бощин А., Стин Б., Йоханссон П. и Паласин М. Р. (2015). Неводные электролиты для натрий-ионных аккумуляторов. Дж. Матер. хим. 3 (1), 22–42. doi:10.1039/C4TA04428B
Полный текст перекрестной ссылки | Google Scholar
Ци, X., Liu, L., Song, N., Gao, F., Yang, G., Lu, Y., et al. (2017). Разработка и сравнительное исследование гибридных структур O3/P2 для натрий-ионных аккумуляторов при комнатной температуре. Приложение ACS Матер. Интерфейсы 9 (46), 40215–40223. doi:10.1021/acsami.7b11282
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Роскилл (2019). Литий: перспективы до 2028 г. . 16-е изд. Роскилл.
Google Scholar
Шин С. М., Ким Н. Х., Сон Дж. С., Ян Д. Х. и Ким Ю.Х. (2005). Разработка процесса извлечения металла из отходов литий-ионных аккумуляторов. Гидрометаллургия 79 (3‒4), 172–181. doi:10.1016/j.hydromet.2005.06.004
CrossRef Полный текст | Google Scholar
Сун В., Цзя X., Ву З., Янга Ю., Чжоуа З., Лия Ф. и др. (2014). Исследование механизма миграции ионов и диффузионной способности катода Na3V2(PO4)2F3, используемого в перезаряжаемых натрий-ионных батареях. Дж. Источники питания 256, 258–263. doi:10.1016/j.jpowsour.2014.01.025
CrossRef Полный текст | Google Scholar
Сунь X., Хао Х., Хартманн П., Лю З. и Чжао Ф. (2019). Риски поставок материалов для литий-ионных аккумуляторов: оценка всей цепочки поставок. Материал. Today Energy 14, 100347. doi:10.1016/j.mtener.2019.100347
CrossRef Полный текст | Google Scholar
Суэйн, Б. (2017). Восстановление и переработка лития: обзор. Отдел. Очист. Технол. 172, 388–403. doi: 10.1016/j.seppur.2016.08.031
CrossRef Полный текст | Google Scholar
UG Survey (2015). «Сводка полезных ископаемых за 2015 год», Сводка полезных ископаемых . Рестон, Вирджиния: Геологическая служба США. doi:10.3133/70140094
Полный текст CrossRef | Google Scholar
Национальный информационный центр полезных ископаемых Геологической службы США (2020 г.). Обзор полезных ископаемых 2020 . . Рестон, Вирджиния: Геологическая служба США.
Google Scholar
Ваалма К., Буххольц Д., Вейл М. и Пассерини С.(2018). Анализ стоимости и ресурсов натрий-ионных аккумуляторов. Nat Rev Mater 3 (4), 1–11. doi:10.1038/natrevmats.2018.13
CrossRef Full Text | Google Scholar
Веласкес-Мартинес В., Сантасало-Аарнио Р. и Серна-Герреро Р. (2019). Критический обзор процессов переработки литий-ионных аккумуляторов с точки зрения экономики замкнутого цикла. Батареи 5 (4), 68. doi:10.3390/batteries5040068
CrossRef Полный текст | Google Scholar
Виньярообан, К., Kushagra, R., Elango, A., Badami, P., Mellander, B.E., Xu, X., et al. (2016). Современные тенденции и будущие проблемы электролитов для натрий-ионных аккумуляторов. Междунар. J. Hydrogen Energy 41 (4), 2829–2846. doi:10.1016/j.ijhydene.2015.12.090
CrossRef Полный текст | Google Scholar
Ван Б., Хан Ю., Ван Х., Бахлаван Н., Пан Х., Ян М. и др. (2018). Аналоги берлинской лазури для аккумуляторных батарей. iScience 3, 110–133. doi:10.1016/j.isci.2018.04.008
Реферат PubMed | Полный текст перекрестной ссылки | Google Scholar
Венткер М., Гринвуд М., Чофор Асаба М. и Лекера Дж. (2019). Оценка критичности сырья и воздействия на окружающую среду современных и постлитий-ионных катодных технологий. J. Energy Storage 26, 101022. doi:10.1016/j.est.2019.101022
CrossRef Полный текст | Google Scholar
Сюй Дж., Ли Д. Х., Клеман Р. Дж., Ю X., Лескес М., Пелл А. Дж. и др. (2014). Выявление критической роли замещения Li в интеркаляционных катодных материалах P2–Na x [Li y Ni z Mn 1– y – z ]O 2 (0 < x y z < 1) для высокоэнергетических Na-ионных аккумуляторов. Хим. Матер. 26 (2), 1260–1269. doi:10.1021/cm403855t
CrossRef Full Text | Google Scholar
Ябуучи Н., Хара Р., Кубота К., Полсен Дж., Кумакура С. и Комаба С. (2014). Новый электродный материал для перезаряжаемых натриевых батарей: Na 2/3 [Mg 0,28 Mn 0,72 ]O 2 типа Р2 с аномально высокой обратимой емкостью. Дж. Матер. хим. 2 (40), 16851–16855. doi:10.1039/C4TA04351K
Полный текст перекрестной ссылки | Google Scholar
Яо Ю., Чжу М., Чжао З., Тонг Б., Фань Ю. и Хуа З. (2018). Гидрометаллургические процессы переработки отработанных литий-ионных аккумуляторов: критический обзор. ACS Sustain. хим. англ. 6 (11), 13611–13627. doi:10.1021/acssuschemeng.8b03545
Полный текст CrossRef | Google Scholar
Ю, Ю., и Мантирам, А. (2018). Прогресс в высоковольтных катодных материалах для перезаряжаемых натрий-ионных аккумуляторов. Доп. Энергетический материал. 8. 2. doi:10.1002/aenm.201701785
CrossRef Full Text | Google Scholar
You, Y., Ву, X.-L., Инь, Y.-X., и Го, Y.-G. (2014). Высококачественные кристаллы берлинской лазури в качестве превосходных катодных материалов для натрий-ионных аккумуляторов при комнатной температуре. Энергетическая среда. науч. 7 (5), 1643–1647. doi:10.1039/C3EE44004D
Полный текст перекрестной ссылки | Google Scholar
Ю М., Инь З., Ян Г., Ван З., Го Х., Ли Г. и др. (2020). Синергия межслойного расширения и емкостного вклада, способствующего хранению ионов натрия в мезопористом углеродном нановолокне, легированном S, N. Дж.Источники питания 449, 227514. doi:10.1016/j.jpowsour.2019.227514
CrossRef Полный текст | Google Scholar
Чжан, Х. (2019). Полианионные катодные материалы для натрий-ионных аккумуляторов. Карлсруэ: Технологический институт Карлсруэ .
Google Scholar
Чжао, Н., Ли, К., и Го, X. (2014). Аккумуляторы Na–O 2 с длительным сроком службы с высокой энергоэффективностью благодаря электрохимическому расщеплению NaO 2 при низком перенапряжении. Физ. хим. хим. физ. 16 (29), 15646–15652.doi:10.1039/C4CP01961J
PubMed Abstract | Полный текст перекрестной ссылки | Google Scholar
Чжао К., Лу Ю. и Чен Дж. (2017). Усовершенствованные органические электродные материалы для перезаряжаемых натрий-ионных аккумуляторов. Доп. Энергия Матер. 7 (8), 1601792. doi:10.1002/aenm.201601792
CrossRef Полный текст | Google Scholar
Чжэн Л., Ли Дж. и Обровац М. Н. (2017). «Кристаллические структуры и электрохимические характеристики стабильных на воздухе Na 2/3 Ni 1/3– x Cu x Mn 2/3 O 2 в натриевых элементах. Хим. Матер. 29 (4), 1623–1631. doi:10.1021/acs.chemmater.6b04769
Полный текст CrossRef | Google Scholar
Zheng, X., Zhu, Z., Lin, X., Zhang, Y., He, Y., Cao, H., et al. (2018). Мини-обзор по переработке металла из отработанных литий-ионных аккумуляторов. Машиностроение 4 (3), 361–370. doi:10.1016/j.eng.2018.05.018
CrossRef Full Text | Google Scholar
Zhu, X., Lin, T., Manning, E., Zhang, Y., Yu, M., Zuo, B., et al. (2018). Последние достижения в области катодных материалов на основе Fe и Mn для литий-ионных и натрий-ионных аккумуляторов. Дж. Нано Рез. 20 (6). doi:10.1007/s11051-018-4235-1
Полный текст CrossRef | Google Scholar
.
 На ее начальной стадии батарея поддается восстановлению и чуть ниже будет указано, как это делается.
На ее начальной стадии батарея поддается восстановлению и чуть ниже будет указано, как это делается. Компоненты разделяются различными физическими и химическими процессами, и все активные материалы и металлы могут быть восстановлены. Прямое восстановление представляет собой низкотемпературный процесс с минимальным потреблением энергии.
Компоненты разделяются различными физическими и химическими процессами, и все активные материалы и металлы могут быть восстановлены. Прямое восстановление представляет собой низкотемпературный процесс с минимальным потреблением энергии.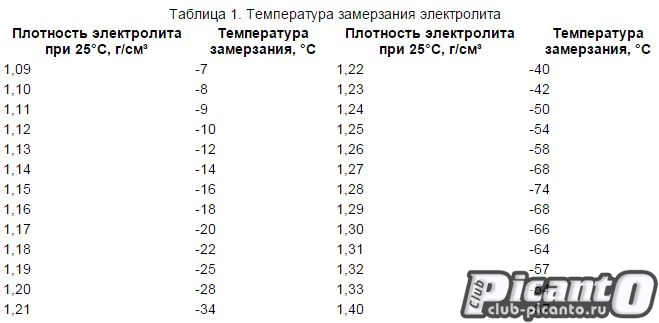 2
2 толщина
толщина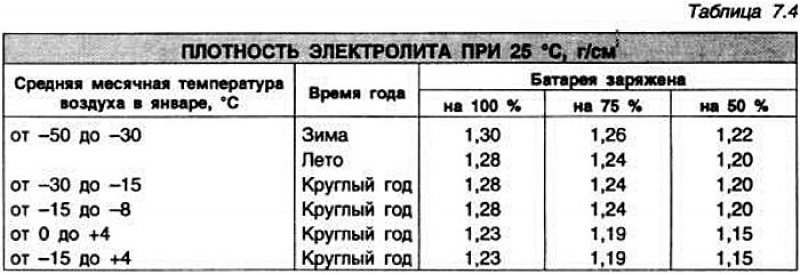 д.
д.